
|
||
|
|
||
|
|
Онлайн книга - Трещина в мироздании | Автор книги - Сэмюел Стернберг , Дженнифер Даудна
Cтраница 23

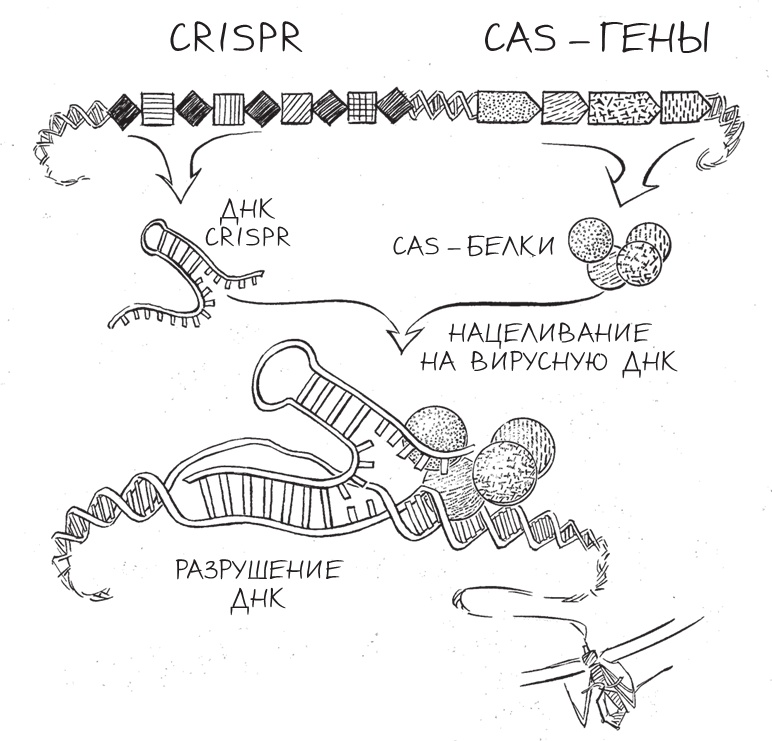
Нацеливание на ДНК посредством РНК CRISPR и Cas-белков Было ясно, что для решения этих вопросов нам нужно выйти за рамки генетического исследования и применить скорее биохимический подход, который позволил бы нам изолировать молекулы, составляющие CRISPR, и изучать их поведение. Кроме того, было необходимо взглянуть на проблему в более широкой перспективе и рассматривать не только сам механизм CRISPR, но и все ассоциированные с CRISPR гены, или cas-гены, которые в бактериальных геномах примыкают к областям CRISPR и, видимо, кодируют особые типы белков – ферменты. Если коротко, этот класс белковых молекул отвечает за катализ всех видов межмолекулярных реакций в клетках. Если бы мы выяснили, что именно делают эти белковые ферменты Cas, мы бы значительно приблизились к пониманию того, как работает CRISPR. Ученые могут многое узнать о функции гена, лишь посмотрев на его химический состав. Фрагменты ДНК, составляющие каждый ген, содержат всю информацию, необходимую клетке для сборки белков из аминокислот. Так как известен генетический код, который используют клетки для перевода четырех “букв” ДНК в двадцать “букв” белка, биологи могут определить последовательность аминокислот в белке, который будет производиться по информации с гена, зная только изначальную последовательность ДНК. Затем, сравнивая полученную последовательность аминокислот со сходными последовательностями у других, лучше изученных белков, ученые могут обоснованно прогнозировать функции многих различных генов. Выдвигая такие многоступенчатые предположения, специалисты в области вычислительной биологии уже выяснили химический состав сотен различных cas-генов, непременно примыкающих к областям CRISPR. Какой бы организм вы ни рассматривали, правило неизменно: если в его геноме содержится ДНК CRISPR, то в непосредственной близости также будут располагаться cas-гены. Это выглядит так, словно CRISPR эволюционировал вместе с cas-генами, и их невозможно представить друг без друга. Мы предположили, что белки, кодируемые этими cas-генами, должны вплотную работать с ДНК CRISPR – или, возможно, с молекулами РНК CRISPR, или даже с ДНК фагов. Было совершенно очевидно: прежде чем мы сможем разобраться в устройстве иммунной системы CRISPR, нам необходимо выяснить, как работают эти гены, и определить биохимические функции белков, которые они вырабатывают. Для начала Блейк выбрал два вида бактерий – Escherichia coli и Pseudomonas aeruginosa, которые содержат определенные типы систем CRISPR. Бактерия E. coli, например, зарекомендовала себя в качестве лучшего друга биохимика. Неважно, чей ген изучает этот биохимик – микроба, растения, лягушки или человека, – работа часто начинается с внедрения этого гена в искусственную мини-хромосому (плазмиду); затем создается специализированный штамм E. coli, который примет плазмиду как часть собственного генома. Совмещая интересующий его ген с другими синтетическими ДНК-инструкциями, биохимик может заставить E. coli не только создавать десятки копий плазмиды в расчете на одну клетку, но и направлять большинство своих ресурсов на конвертирование информации с изучаемого гена в тысячи копий белка, который тот кодирует. Таким образом биохимик практически превращает E. coli в своего рода микроскопический промышленный биореактор, запрограммированный на массовую выработку определенных белков. Блейк быстро сконструировал плазмиды из отдельных ассоциированных с CRISPR генов, скопировав последние из геномов E.coli и P. aeruginosa. Собрав десятки штаммов E. coli, которые он “научил” использовать плазмиды как часть своего генетического материала, Блейк начал литрами выращивать культуры каждого из созданных штаммов, чтобы наработать достаточно Cas-белков для своих экспериментов. Давая бактериям ночь на размножение, по утрам Блейк выливал содержимое колб с культурами в большие емкости и отделял клетки от жидкой питательной среды в больших скоростных центрифугах, в которых клетки подвергались воздействию силы, в четыре тысячи раз большей, чем сила земного притяжения. Затем, работая с каждым штаммом по отдельности, он помещал клетки в небольшое количество солевого раствора и подвергал эту жижу воздействию высокоэнергетических звуковых волн, которые резко разрывали клетки, высвобождая их содержимое – в том числе и выработанные ими Cas-белки. После отделения лишнего материала – разрушенных мембран, вязких ДНК и прочего клеточного “мусора” – у Блейка оставалось несколько тысяч бактериальных белков, из которых ему нужен был только один: Cas-белок. Но благодаря хитроумному строению плазмиды Cas-белок содержал особенный химический ярлык, или придаток, который отличал его от остальных тысяч белков. С помощью определенной стратегии очистки (а также проведя несколько раундов дополнительной очистки) Блейк смог отделить этот молекулярный придаток и получить чистые высококонцентрированные образцы каждого из Cas-белков, которые мы хотели изучать. Когда Cas-белки оказались в его распоряжении, Блейк наконец смог проводить различные эксперименты для изучения того, что именно делают эти ферменты. Нашим первым вкладом в область изучения CRISPR была публикация о следующем открытии: мы обнаружили, что белковый фермент под названием Cas1 мог разрезать ДНК [67] таким образом, что это, возможно, помогало вставлять новые фрагменты ДНК фага в массив CRISPR на стадии формирования памяти иммунной системы. Это приблизило нас к пониманию того, каким образом CRISPR “ворует” кусочки ДНК у атакующих фагов и встраивает эту генетическую информацию в свою собственную, закладывая основу для двух фаз иммунного ответа: наведения на цель и ее уничтожения. Приблизительно на этом этапе Блейк привлек к работе над проектом магистрантку Рэйчел Хорвитц, и вместе они сделали еще одно открытие. Работая со вторым белковым ферментом, Cas6, Рэйчел и Блейк обнаружили, что он, как и Cas1, функционирует в качестве своего рода химического колуна [68]. Однако в случае Cas6 задача заключалась в том, чтобы избирательно и методично разрезать длинные молекулы РНК CRISPR на более короткие куски, которые могли бы быть использованы для нацеливания на ДНК фага. По мере того как мы и другие исследователи собирали детали CRISPR-пазла, медленно, но верно начинала вырисовываться общая картина. В ней мы уже могли различить ответы на некоторые вопросы, которые поставили перед собой в начале работы над проектом. Мы видели, что нам предстоит открыть еще множество функций Cas-белков. В ходе исследования мы обнаруживали все больше и больше таких белков, которые оказывались ферментами, разрезающими ДНК или РНК, – а значит, вероятно, играли в иммунном ответе CRISPR роль, похожую на роль Cas1 и Cas6.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно