
|
||
|
|
||
|
|
Онлайн книга - Происхождение жизни. От туманности до клетки | Автор книги - Михаил Никитин
Cтраница 38

Копирование РНК путем крупноблочной сборки
Стало понятно, что надо искать другие подходы к копированию РНК. Например, процесс копирования мог поначалу происходить путем сшивания концов коротких цепей, а не одиночных нуклеотидов. Обзор Карлоса Брионеса с соавторами (2009) суммирует главные открытия в этой области. В этом сценарии первые РНК длиной 20–30 нуклеотидов образуются при случайной полимеризации на минералах. Многие из них имеют участки, комплементарные другой части молекулы, и образуют шпильки (рис. 9.3). Среди них были первые рибозимы, проводящие реакцию сшивания концов двух цепей РНК, под названием «лигазы». Они сшивали некоторые РНК друг с другом, что приводило к появлению, во-первых, более активных лигаз, а во-вторых, эти лигазы лучше узнавали те короткие РНК, из которых могли быть построены их собственные копии. По мере роста размеров и сложности РНК среди лигаз могли появиться и рибозимы-полимеразы. 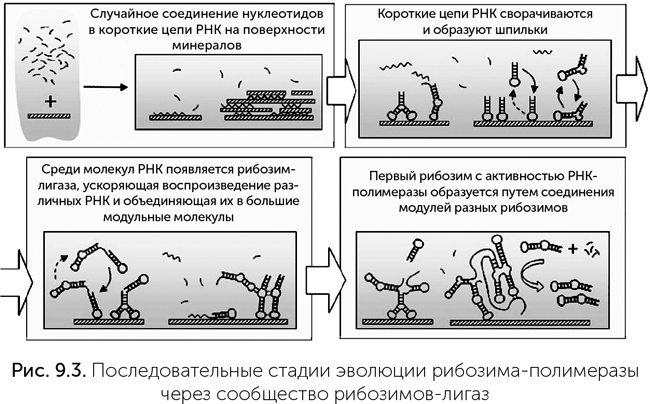
Такой сценарий решает часть проблем, которые были в сценарии случайного появления полимеразы. Во-первых, рибозимы-лигазы гораздо проще и короче, чем рибозимы-полимеразы: при комнатной температуре хорошо работают лигазы длиной 40–50 нуклеотидов, а во льду – даже более короткие фрагменты, вплоть до 29 нуклеотидов (Vlassov et al., 2004). Молекулы РНК таких размеров реально получить при случайной сшивке нуклеотидов без помощи рибозимов. Во-вторых, лигазы могут сшивать две разные функциональные молекулы РНК, образуя более крупные модульные рибозимы, – путь усложнения, малодоступный для рибозимов-полимераз. В-третьих, в экспериментах рибозимы-лигазы склонны образовывать сообщества, в которых разные лигазы ускоряют сборку друг друга, поддерживая более сложную и разнообразную систему, чем один рибозим-полимераза. Более того, такие сообщества выигрывают в конкуренции с эгоистичной лигазой, собирающей только свои копии. В экспериментах Трейси Линкольн и Джеральда Джойса пара лигаз собирала копии друг друга (Lincoln, Joyce, 2009) и удваивала свою численность менее чем за час, тогда как полимеразы не могут собрать свою копию и за сутки! Более того, добавив в систему несколько версий «сырья» – коротких цепочек РНК, они добились конкуренции разных вариантов рибозимов-лигаз и начала эволюции среди них. Единственный недостаток известных сообществ лигаз, не позволяющий признать их окончательным решением проблемы копирования в мире РНК, – это необходимые для них исходные материалы. Лигазы Линкольн и Джойса так же, как их аналоги, полученные другими учеными, требуют довольно длинных фрагментов РНК, около 20 нуклеотидов, для построения из них собственных копий. Если материал для лигаз поставляется случайным соединением нуклеотидов на глине, то вероятность получения нужного 20-нуклеотидного фрагмента РНК будет крайне мала – около одной триллионной. Лигазы, хорошо работающие с кусочками РНК в три – пять нуклеотидов, пока получить не удается. Интересный вариант содружества лигаз был получен в работе Щепанского и Джойса (Sczepanski, Joyce, 2014). Они отступили от принципа хиральной чистоты и сделали рибозим из нуклеотидов с «левыми» молекулами рибозы, отбирая его на способность сшивать обычные РНК с «правой» рибозой. В этом случае звенья рибозима не образуют комплементарных пар с теми молекулами, которые он сшивает. Подобные взаимодействия приводят к застреванию молекул РНК в обычных рибозимах-полимеразах и лигазах и сильно замедляют их работу. «Левый» рибозим из 83 нуклеотидов оказался очень хорошей лигазой, способной построить свою зеркальную копию из 11 коротких фрагментов РНК по 7–11 нуклеотидов. Зеркальная копия, в свою очередь, так же эффективно строит исходный «левый» рибозим из «левых» коротких РНК. Такой способ копирования был назван «кросс-хиральная репликация». Как и некоторые другие лигазы, этот рибозим может по совместительству «подрабатывать» полимеразой: он достраивает РНК-затравку, присоединяя к ней до шести нуклеотидных звеньев, причем к «правой» затравке присоединяются только «правые» нуклеотиды из смеси, а к «левой» – «левые». Этот эксперимент заставляет задуматься об истории хиральной чистоты: может быть, мир РНК сначала использовал левые и правые нуклеотиды в равной мере, а хиральная чистота возникла позже, с переходом к белкам? Авторы надеются в ближайшие пару лет сделать из этой лигазы кросс-хиральную полимеразу, которая будет строить из отдельных нуклеотидов свои зеркальные отражения. Посмотрим, что у них получится. Итак, ни рибозимы-полимеразы, ни рибозимы-лигазы, известные на сегодняшний день, не обеспечивают устойчивого копирования РНК из доступных в окружающей среде древней Земли компонентов – отдельных нуклеотидов и их цепочек длиной до пяти-восьми звеньев. Чтобы запустить копирование, а следовательно, конкуренцию и естественный отбор, необходимы какие-то другие способы копирования РНК. РНК копируются внешними силами
Самопроизвольное соединение активированных нуклеотидов, с которого мы начали эту главу, может происходить не только на глине, но и на однонитевых молекулах РНК, работающих в качестве матрицы. Достижения и проблемы в этой области обобщены в обзоре Джека Шостака (Szostak, 2012). Еще в 1987 году было достигнуто неферментативное копирование РНК длиной 14 нуклеотидов. Использовались нуклеотид-метилимидазол-фосфаты и водный раствор с высокой концентрацией солей магния (Acevedo, Orgel, 1987). В последующие годы это направление исследований было практически заброшено, так как ученые переключились на искусственный отбор рибозимов. Но в последние годы Джек Шостак вернулся к неферментативному копированию, причем с новыми идеями – он пытается проводить его внутри протоклеток, т. е. пузырьков, окруженных липидной мембраной. Недавно ученицей Шостака Катаржиной Адамалой было осуществлено копирование РНК внутри протоклеток (Adamala, Szostak, 2013). Копирование РНК без помощи ферментов имеет много недостатков, которые нам знакомы по рибозимам-полимеразам: • в конце копирования, как и у полимеразы, образуется устойчивая двунитевая РНК, которую надо как-то расплести для следующего цикла копирования; • скорость и точность неферментативного копирования еще хуже, чем с рибозимами: ошибок – около 10 %, а на присоединение одного нуклеотида уходит более часа. У неферментативного копирования есть и другие проблемы, которые не свойственны рибозимам-полимеразам: • при копировании без ферментов связи между нуклеотидами образуются по-разному. Как в клеточных РНК, так и в продуктах рибозимов-полимераз, фосфатные мостики всегда связывают третий углеродный атом одного остатка рибозы с пятым атомом другого (3' – 5' – фосфодиэфирная связь, см. рис. 9.1). Без ферментов же наравне с 3' – 5' связями образуются неправильные 2' – 5' связи, и долго было непонятно, насколько это мешает появлению активных рибозимов; • неферментативное копирование требует высокой концентрации магния, что приводит к постепенному разрушению как РНК-матрицы, так и активированных нуклеотидов. Нуклеотиды теряют фосфатные группы и превращаются в нуклеозиды, которые сами непригодны для построения цепи РНК и, хуже того, конкурируют с нуклеотидами за место на копируемой цепи РНК;
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно