
|
||
|
|
||
|
|
Онлайн книга - Карнавал молекул | Автор книги - Михаил Левицкий
Cтраница 23

Процедура разделения монет на две группы мало похожа на химическую реакцию. Для того чтобы достичь сходства, поместим всю исходную кучку монет в мешочек и начнем встряхивать. Далее допустим, что при встряхивании монеты разного достоинства «слипаются» и из одной 50-копеечной и пяти 10-копеечных образуется рубль. В результате после долгого встряхивания в мешочке окажутся только рубли (если исходное соотношение 10- и 50-копеечных монет было 5:1). Теперь, очевидно, вам понятно, что энтропия содержимого в мешочке понизилась, стало меньше «беспорядка», поскольку получились только монеты одного достоинства и их количество меньше, чем было до встряхивания (рис. 2.59). 
Рассмотренная ситуация с монетами очень напоминает реакцию получения уксусной кислоты из метана и углекислого газа, где из двух молекул получилась одна. Очевидно, что эта реакция проходит с уменьшением энтропии. Во многих случаях найденное нами правило сохраняется: если в правой части химического уравнения молекул меньше, чем в левой (стехиометрические коэффициенты, стоящие у реагентов, тоже учитывают), то реакция проходит с уменьшением энтропии. Естественно, если в правой части уравнения молекул больше, чем в левой, то энтропия в результате реакции, скорее всего, возрастает. На практике энтропийный фактор оценивают не на глазок, как это делали мы (с какой стороны уравнения участвует больше молекул), а по расчетам. Часто бывает, что в правой и левой части уравнения одинаковое количество молекул, в этом случае расчет становится необходимым. Для рассматриваемой реакции проведенный расчет подтверждает наши предположения: энтропия в результате реакции снижается на величину 220 Дж/градус. Много это или мало? В нашем случае это не так существенно, поскольку важно лишь то, что она снижается, что создает для реакции непреодолимый барьер. На основании чего можно сделать такой категоричный вывод? Существует всего четыре правила, которые позволяют сказать, пойдет реакция или не пойдет. Мы с нашей реакцией попали в самую неудачную ситуацию. Четыре правила для химика Для того чтобы определить, возможно ли протекание реакции, надо сопоставить величину теплового эффекта и изменение энтропии. Существует всего четыре варианта. 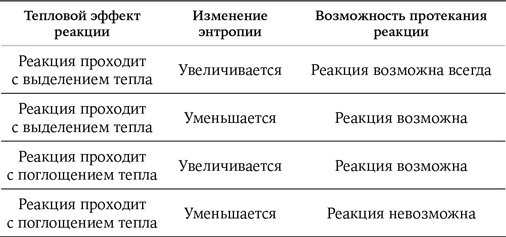
Расчеты показали, что наша реакция эндотермическая и к тому же идет с понижением энтропии, т. е. наш вариант – четвертый, а значит, реакция невозможна. Не помогут никакие катализаторы, давление, нагревание, охлаждение, перемешивание и все остальные лабораторные приемы. А что представляют собой остальные три варианта в реальности? Для первого варианта наиболее убедительный пример – тринитротолуол (тол). Он может разлагаться со взрывом, реакция отчетливо экзотермическая. Кроме того, из одной молекулы тринитротолуола образуется по крайней мере четыре соединения – СО2, N2, NO, Н2О. Следовательно, энтропия возрастает. К этому же варианту относятся все процессы горения углеводородного топлива, в результате чего образуются газообразные продукты СО2 и Н2О. Грустный четвертый случай мы уже рассмотрели, а два промежуточных наиболее интересны, поскольку чаще всего встречаются в химической практике. В обоих этих случаях надо сопоставить количественные величины теплового эффекта реакции и энтропии. Поскольку размерность теплового эффекта – калории, а у энтропии – калории/градус (в расчете на один моль вещества), то следует величину энтропии умножить на значение абсолютной температуры, при которой происходит процесс, после этого размерности станут одинаковыми и величины можно будет сравнивать. Обратите внимание, во втором и третьем варианте оба фактора действуют в противоположных направлениях. Во втором варианте выделение тепла способствует легкому протеканию реакции, а уменьшение энтропии делает ее менее вероятной. В третьем варианте оба фактора «меняются местами». Конечный результат зависит от того, кто кого перетянет. Вот пример реакции по второму варианту – взаимодействие оксида кальция с водой (гашение извести): CaO + H2O == Ca(OH)2. Из двух соединений получается одно, т. е. энтропия уменьшается, но зато реакция при комнатной температуре идет с сильным разогревом (экзотермическая), энергетический фактор пересиливает энтропийный, реакция становится возможной. Существуют реакции и по третьему варианту – это получение негашеной извести: CaCO3 = CaO + CO2. Расчет показывает, что реакция эндотермическая. Как мы знаем, при комнатной температуре она не идет; обычный мел спокойно хранится, не разлагаясь. Однако реакцию провести можно, поскольку в результате ее увеличивается энтропия (из одного соединения получаются два). Ранее было сказано, что при сопоставлении двух сравниваемых величин энтропийный фактор умножают на абсолютную температуру. Таким образом, мы можем увеличивать роль энтропийного фактора, повышая температуру. При 830 °С обе величины сравняются, а при дальнейшем повышении температуры реакция пойдет в нужном нам направлении, т. е. энтропийный фактор перетянет и мел превратится в негашеную известь СаО. Все, о чем было рассказано выше, можно считать введением в термодинамику – науку о превращении энергии, но все же остался нерешенным вопрос: что делать с невозможной реакцией и при чем здесь акулы и рыбы-прилипалы? Сделать невозможное возможным Итак, реакция, показанная в самом начале нашего рассказа, термодинамически запрещена, тем не менее осуществить намеченное превращение можно, если воспользоваться обходным путем. Знающий химик предложит такую последовательность реакций: ● 1-я стадия – бромирование метана. ● 2-я стадия – получение магнийорганического соединения (реакция Гриньяра), когда атом Mg встраивается между атомами С и Br. ● 3-я стадия – взаимодействие магнийорганического соединения с СО2, при этом происходит встраивание СО2 между атомами С и Mg. ● 4-я стадия – взаимодействие соединения, полученного на третьей стадии, с HBr. В итоге образуется уксусная кислота и побочный продукт – MgBr2 (рис. 2.60). 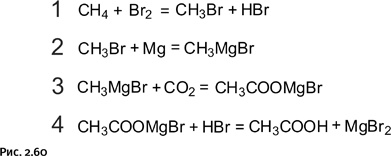
Схема несколько громоздкая, но зато все реакции реально осуществимы, и расчеты показывают, что они термодинамически разрешены. Окончательная ясность возникает, если все четыре стадии просуммировать, вычеркнув (или, как говорят математики, сократив) те соединения, которые присутствуют в правой и левой частях уравнений в одинаковых количествах, а затем представить оставшиеся (не зачеркнутые) реагенты в виде уравнения (рис. 2.61). 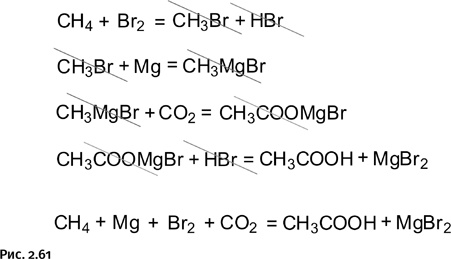
Полученное в результате суммирования окончательное уравнение нагляднее будет представить в виде двух реакций (рис. 2.62). Первая реакция – та, с которой мы начали наш рассказ, а вторая – взаимодействие магния и брома с образованием бромида магния. Ее экзотермичность весьма высока, практически 420 кДж/моль (1 кДж = 1000 Дж), что с лихвой перекрывает и эндотермичность первой реакции, а также то, что в каждой из двух реакций энтропия уменьшается (из двух соединений получается одно). Именно вторая реакция играет роль мощной акулы, которая везет на себе слабенькую рыбу-прилипалу, т. е. термодинамически невозможную реакцию. Энергия, выдаваемая этой «акулой», постепенно расходуется на каждой из четырех стадий.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно