
|
||
|
|
||
|
|
Онлайн книга - От атомов к древу. Введение в современную науку о жизни | Автор книги - Сергей Ястребов
Cтраница 27

Возвращаясь к началу этой главы, мы теперь можем уточнить, что липиды на самом деле довольно редко бывают полностью гидрофобными. Чаще они амфифильны. Многие их биологические свойства именно с этим и связаны. Жиры
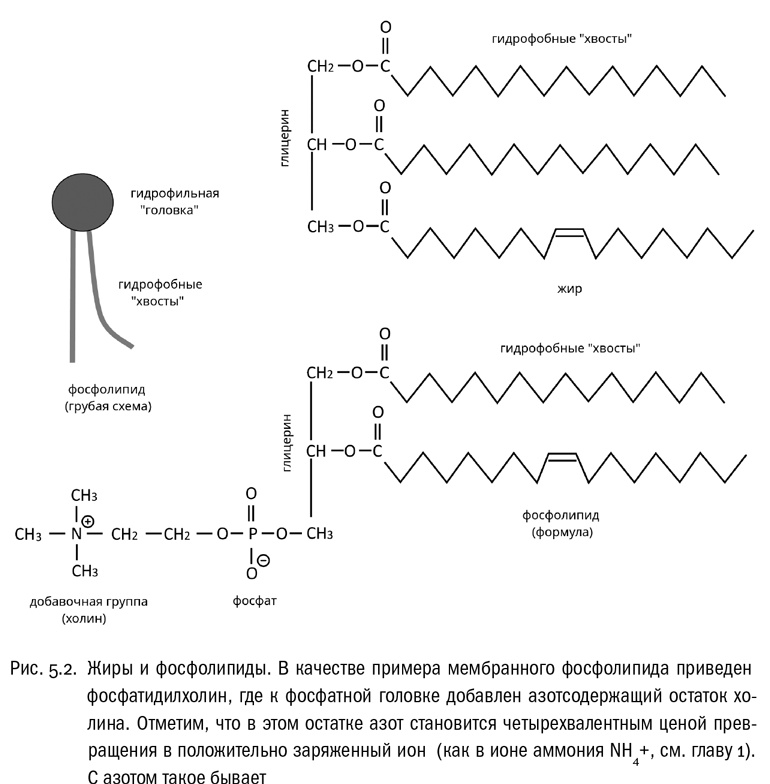
Теперь еще раз вспомним, что любая карбоновая кислота (в том числе и жирная) в принципе может образовать с любым спиртом сложный эфир. При этом от кислоты отщепится –OH, от спирта –H, они образуют воду, а остатки кислоты и спирта замкнутся в единую молекулу со сложноэфирной группой –CO–O– посредине (см. рис. 5.2). Спиртом, участвующим в этой реакции, вполне может оказаться и глицерин, у которого гидроксильных групп целых три (см. главу 1). Сложный эфир глицерина и трех жирных кислот называется жиром. Молекула жира имеет “головку” (остаток глицерина) и сразу три углеводородных “хвоста” (см. рис. 5.2). На самом деле жиры стали известны людям гораздо раньше, чем их исходные компоненты. Например, желтый костный мозг, который наверняка извлекали древние люди из трубчатых костей крупных млекопитающих, — это в основном жир. По опыту мы все знаем, что жир — это вещество животного или растительного происхождения, нерастворимое в воде, жирное на ощупь и оставляющее на бумаге характерные жирные пятна. Жиры, остающиеся при комнатной температуре жидкими, принято называть маслами. Иногда в разговорах о химическом составе пищи понятие “липиды” для простоты заменяют понятием “жиры”. Теперь мы знаем, что это неточность. Жиры — и вправду ценные питательные вещества, но это далеко не единственные липиды, которые важны в этой роли. Например, холестерин — липид, но никакой не жир. С участием насыщенных жирных кислот образуются насыщенные жиры, а с участием ненасыщенных кислот, соответственно, ненасыщенные. В растительных маслах гораздо больше ненасыщенных жиров, чем в животных. Хотя в целом и там и там есть и те и другие, отличается только их вклад. Жиры — очень ценные источники энергии. Молекула жира может дать в два раза больше энергии, чем молекула углевода, имеющая такой же размер. Объясняется это вот чем. Процесс, путем которого мы получаем энергию из питательных веществ, — это, в сущности, окисление, то есть присоединение кислорода ко всем атомам водорода и углерода, до которых можно дотянуться. Все другие связи, образуемые этими атомами, при окислении разрываются, а его конечными продуктами становятся вода (H2O) и углекислота (CO2). Проблема в том, что в молекулах углеводов значительная часть атомов уже соединена с кислородом, так что окислять их дальше некуда (ну, или почти некуда). В молекулах жиров, где есть длинные жирнокислотные “хвосты”, таких атомов гораздо меньше. А потому и энергии из окисления жиров можно извлечь больше. Кроме того, что жиры энергоемки, они еще и удобны для компактного хранения, поэтому животные (включая человека) часто используют их в качестве запасных веществ. Известно, что организм склонен реагировать на длительный стресс усилением отложения жира — это одна из причин так называемого стресс-индуцированного ожирения. Конечно, это эволюционно обусловленная реакция: с точки зрения нашего организма чем тяжелее и неопределеннее условия жизни, тем выше вероятность того, что запасные вещества в обозримом будущем пригодятся. Мы уже знаем, что одним из конечных продуктов окисления питательных веществ является вода. Поэтому жировые отложения могут фактически служить запасом не только энергии, но и воды, которая все равно неизбежно выделяется при их переработке. Это особенно важно для пустынных животных вроде верблюдов. Горб верблюда содержит только жир, но при полном окислении этот жир (как и любой другой) превращается в углекислоту и воду. Углекислоту верблюд выдыхает, а воду оставляет в своем теле, чтобы добро не пропадало. Некоторые тушканчики, тоже живущие в пустынях или полупустынях, запасают жир подобно верблюдам и в тех же целях, но не в горбе, а в хвосте. Они так и называются — толстохвостые тушканчики.
Фосфолипиды
А теперь познакомимся еще с одним важным для нас веществом — фосфорной кислотой, имеющей формулу H3PO4. Структура у нее довольно простая. Мы уже знаем, что валентность фосфора — 5 (см. главу 1). В фосфорной кислоте к атому фосфора присоединены четыре атома кислорода, один двойной связью, а все остальные одинарными. К этим последним присоединены атомы водорода. Когда фосфорная кислота находится в растворе, атомы водорода (вернее, протоны) могут отрываться, превращая фосфорную кислоту в анион. Здесь, как и раньше, надо иметь в виду, что “фосфорная кислота” и “фосфат” (то есть ее анион либо соль) в биохимии почти синонимы. В подавляющем большинстве случаев эти понятия свободно заменяются друг на друга. Очень часто название “фосфорная кислота” заменяют на “фосфат” просто для краткости. Фосфорная кислота может участвовать в образовании сложных эфиров точно так же, как и карбоновые кислоты (см. рис. 5.2). Сложный эфир глицерина, двух жирных кислот и фосфорной кислоты называется фосфолипидом. Это — исключительно важный для биологии класс соединений. Можно сказать, что фосфолипид — это жир, у которого вместо одного из остатков жирных кислот тем же способом присоединен фосфат. Такая молекула состоит из гидрофильной “головки” (включающей остатки глицерина и фосфата) и двух гидрофобных “хвостов” (жирных кислот). При фосфате бывают еще добавочные боковые цепи, у разных фосфолипидов разные. Два особенно широко распространенных фосфолипида — фосфатидилхолин и фосфатидилсерин. В фосфатидилхолине дополнительной боковой цепью при фосфате служит холин, небольшая азотсодержащая органическая молекула (см. рис. 5.2Г). А в фосфатидилсерине к фосфату присоединена аминокислота серин. В другие биохимические детали нам тут вдаваться не стоит, общие свойства фосфолипидов все равно гораздо важнее. А состоят они в том, что любой фосфолипид — это ярко выраженная амфифильная молекула, состоящая, если совсем уж попросту, из одной большой гидрофильной “головки” и двух длинных гидрофобных “хвостов”. Знакомство с мембраной
Мы уже знаем, что никакие липиды не растворяются в воде. Что же будет, если их с водой все-таки принудительно смешать? Правильно: молекулы липидов начнут слипаться друг с другом своими гидрофобными частями, как бы защищая их от контакта с водой, и это называется гидрофобным взаимодействием. А гидрофильные части молекул будут, наоборот, втягиваться в воду, ориентируясь в сторону ее толщи. Это типичное поведение амфифильных веществ. Будем для определенности называть гидрофильную часть любого липида “головкой”, а гидрофобную — “хвостом”. И мы увидим, что при смешивании с водой молекулы липидов могут группироваться тремя способами (см. рис. 5.3): * мицелла — шарообразное скопление, где “хвосты” обращены внутрь, минимизируя контакт с водой, а “головки” — наружу. Ничего, кроме самих молекул липидов, мицелла не содержит. Мицеллы особенно легко образуются из молекул, где “головка” по диаметру превосходит “хвост”, то есть молекула имеет форму конуса. Таковы, например, молекулы жирных кислот;
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно