
|
||
|
|
||
|
|
Онлайн книга - Вселенная. Курс выживания среди черных дыр, временных парадоксов, квантовой неопределенности | Автор книги - Дэйв Голдберг , Джефф Бломквист
Cтраница 3

Насколько мы можем судить сейчас, одиночный электрон похож на того самодовольного чиновника по Резерфорду, то есть на точку, и вращается по орбите вокруг ядра атома водорода по радиусу примерно в 100 000 раз больше диаметра ядра. Ядро имеет положительный электрический заряд, а электрон – отрицательный, и это значит, что между ними есть сила притяжения, которая аналогична силе гравитации, удерживающей Землю на солнечной орбите. Это, в свою очередь, означает, что атомы – это в основном пустое пространство. Если представить себе атомное ядро размером с теннисный мяч, то электрон будет меньше пылинки, летящей за километр от этого мяча. Такие цифры весьма удивляют, потому что твердая материя явно не кажется нам такой уж пустой. Резерфордовские атомные ядра поставили перед физиками того времени ряд проблем. Например, было хорошо известно, что электрон должен терять энергию при движении по орбите вокруг ядра, поскольку все объекты с электрическим зарядом отдают энергию, двигаясь по искривленным траекториям. Эта идея лежит в основе работы радиопередатчиков: электроны колеблются, в результате чего создаются электромагнитные радиоволны. Генрих Герц изобрел радиопередатчик в 1887 году, и ко времени открытия Резерфордом атомного ядра уже существовала коммерческая радиостанция, отправлявшая сообщения через Атлантический океан – из Ирландии в Канаду. Таким образом, уже никто не удивлялся теории вращающихся по орбите зарядов и излучения радиоволн, но это смущало тех, кто пытался объяснить, как же электроны остаются на орбите вокруг ядра. Столь же необъяснимый феномен представлял собой свет, который испускали разогреваемые атомы. Еще в 1853 году шведский ученый Андерс Ангстрем пропустил искру через трубку, наполненную водородом, и проанализировал полученный свет. Можно было предположить, что газ будет светиться всеми цветами радуги; в конце концов, что такое Солнце, как не светящийся газовый шар? Вместо этого Ангстрем обнаружил, что водород светится тремя отчетливыми цветами: красным, сине-зеленым и фиолетовым, давая три чистые узкие дуги, как у радуги. Вскоре было выявлено, что так ведут себя все химические элементы. У каждого из них есть уникальный цветовой штрихкод. К тому времени как Резерфорд выступил по поводу атомного ядра, ученый Генрих Кайзер завершил работу над шеститомным справочником из 5000 страниц, озаглавленным Handbuch der Spectroscopie («Справочник по спектроскопии»): он описывал все цветные светящиеся линии известных элементов. Вопрос, конечно, зачем? И не только «Зачем, профессор Кайзер?» (наверное, за обедом над его фамилией нередко шутили), но и «Почему так много цветных линий?». Более 60 лет наука, получившая название спектроскопии, была эмпирическим триумфом и теоретическим провалом. В марте 1912 года датский физик Нильс Бор, очарованный проблемой строения атома, отправился в Манчестер для встречи с Резерфордом. Позже он отмечал, что попытки расшифровать внутреннее строение атома по данным спектроскопии были чем-то сродни выведению базовых постулатов биологии из раскраски крыла бабочки. Атом Резерфорда с его моделью в духе Солнечной системы дал Бору необходимую подсказку, и в 1913 году он уже опубликовал первую квантовую теорию строения атома. У этой гипотезы, конечно, были свои проблемы, но она содержала несколько важнейших идей, подстегнувших развитие современной квантовой теории. Бор заключил, что электроны могут занимать лишь определенные орбиты вокруг ядра, а орбитой с самой низкой энергией будет ближайшая. Он утверждал также, что электроны способны перепрыгивать с орбиты на орбиту. Они переходят на более отдаленную орбиту, когда получают энергию (например, от искры в трубке), а затем продвигаются ближе к центру, одновременно излучая свет. Цвет этого излучения непосредственно определяется разностью энергий электрона на этих двух орбитах. Рис. 2.1 иллюстрирует основную идею; стрелка показывает, как электрон перепрыгивает с третьего энергетического уровня на второй, испуская свет (представленный волнистой линией). В модели Бора электрон может двигаться вокруг протона (ядра атома водорода) лишь по одной из особых, «квантованных» орбит; движение по спирали просто запрещено. Таким образом, модель Бора позволила ему вычислить длины волн (то есть цвета) света, который наблюдался Ангстремом: они соответствовали прыжку электрона с пятой орбиты на вторую (фиолетовый цвет), с четвертой орбиты на вторую (сине-зеленый цвет) и с третьей на вторую (красный цвет). Модель Бора к тому же корректно предсказывала существование света, который должен испускаться при переходе электрона на первую орбиту. Этот свет – ультрафиолетовая часть спектра, невидимая человеческому глазу. Поэтому не видел ее и Ангстрем. Однако в 1906 году ее зафиксировал гарвардский физик Теодор Лайман, и эти данные замечательно описывались моделью Бора. 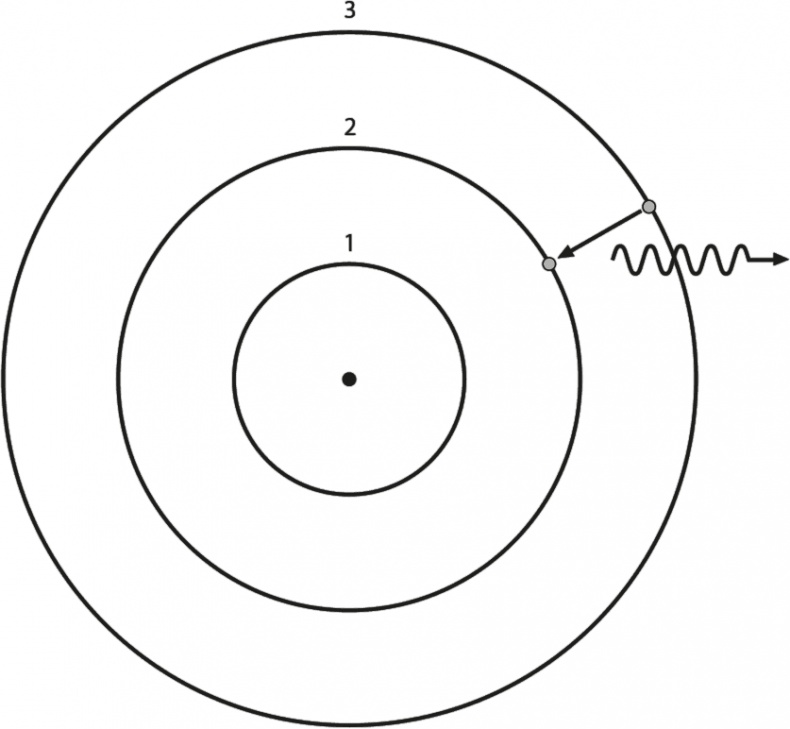
Рис. 2.1. Модель атома Бора, иллюстрирующая испускание фотона (волнистая линия) в результате перехода электрона с одной орбиты на другую (обозначен стрелкой) Хотя Бор не сумел распространить свою модель дальше атома водорода, выдвинутые идеи можно было применить и к другим атомам. Например, если предположить, что у атомов каждого элемента набор орбит уникален, они будут испускать световые лучи лишь определенного цвета. Таким образом, эти цвета служат своего рода «отпечатками пальцев» атома, и астрономы, разумеется, немедленно воспользовались уникальностью спектральных линий атомов для определения физического состава звезд. Модель Бора – неплохое начало, но всем была ясна ее недостаточность: например, почему электроны не могут двигаться по спирали, когда известно, что они должны терять энергию, испуская электромагнитные волны (идея, получившая реальное подтверждение с появлением радио)? И почему орбиты электрона изначально квантуются? И как насчет более тяжелых, чем водород, элементов: что делать для понимания их строения? Но какой бы несовершенной ни казалась теория Бора, это был критически важный шаг и пример того, как порой учеными достигается прогресс. Нет никакой причины складывать оружие перед лицом озадачивающих и порой ставящих в тупик фактов. В подобных случаях ученые часто делают так называемый анзац – прикидку, или, если угодно, правдоподобное допущение, а затем переходят к вычислению его последствий. Если предположение работает, то есть получающаяся теория согласуется с экспериментальными данными, то можно с большей уверенностью вернуться к изначальной гипотезе и пытаться более детально в ней разобраться. Анзац Бора 13 лет оставался успешным, но не до конца объясненным. Мы вернемся к истории этих ранних квантовых идей на последующих страницах книги, но сейчас перед нами лишь множество странных результатов и вопросы с неполными ответами – как и перед основоположниками квантовой теории. Если резюмировать, то Эйнштейн, следуя за Планком, предположил, что свет состоит из частиц, но Максвелл уже показал, что свет ведет себя как волна. Резерфорд и Бор прокладывали путь к пониманию строения атома, но поведение электрона внутри атома не согласовывалось ни с одной из известных в то время теорий. А разнообразные явления, носящие общее название радиоактивности, при которой атомы спонтанно делятся на части по невыясненным причинам, оставались загадкой – во многом потому, что вносили в физику волнующий элемент случайности. Сомнений не оставалось: в субатомном мире грядет что-то странное.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно