
|
||
|
|
||
|
|
Онлайн книга - Происхождение жизни. От туманности до клетки | Автор книги - Михаил Никитин
Cтраница 31

Земля отличается от Титана в нескольких отношениях. Во-первых, она в 10 раз ближе к Солнцу и получает в 100 раз больше ультрафиолетовых лучей на каждый квадратный метр атмосферы. Во-вторых, она гораздо теплее, чем промерзший до –170 °С Титан, и в ее атмосфере есть еще водяной пар и углекислый газ. Поэтому на древней Земле метан в атмосфере реагировал не только с азотом, но и с углекислым газом и водой, образуя формальдегид (CH2O). В-третьих, на Земле идут (и почти всегда шли) дожди из жидкой воды, поэтому продукты фотолиза метана не накапливаются в виде дымки, а растворяются в каплях воды и выпадают с дождем. И синильная кислота, и формальдегид хорошо растворимы в воде и быстро вымываются дождями из атмосферы (рис. 7.3). Поэтому на поверхность древней Земли регулярно поступали те органические вещества, из которых в принципе можно построить аминокислоты, сахара и нуклеотиды: формальдегид, цианид, цианамид и цианоацетилен. Хотя мы привыкли считать цианид сильнейшим ядом, на самом деле он блокирует только кислородное дыхание. Анаэробные (живущие без кислорода) бактерии могут им питаться, и, как мы вскоре увидим, цианид является отличным сырьем для производства азотистых оснований и РНК на заре жизни. 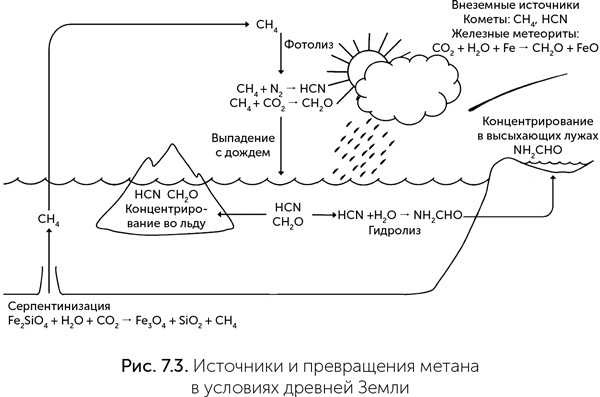
Кроме фотохимических реакций метана есть и другие источники цианида и формальдегида. Цианид обнаруживается в газах и испарениях геотермальных полей, например на склонах Мутновской сопки на Камчатке. Формальдегид образуется из углекислого газа и паров воды при разрядах молний и при контакте атмосферы с горячим металлическим железом (обломки упавших метеоритов и включения железа в вулканических лавах) (Cleaves, 2008). Цианид постепенно реагирует с водой и превращается в формамид (NH2CHO). Как мы увидим, формамид тоже может быть хорошим предшественником нуклеотидов, кроме того, он отличается высокой температурой кипения (218 °C) и поэтому может накапливаться в высыхающих лужах после дождя. Химия цианидно-формальдегидных дождей
Итак, для построения сложных органических молекул на поверхности древней Земли у нас есть формальдегид, цианид и его производные. Что и как можно сделать из этих составляющих? Еще в 1865 году А. М. Бутлеровым была открыта так называемая формозная реакция: водный раствор формальдегида (СH2O) с добавлением гидроокиси кальция (известковая вода) при небольшом нагревании превращается в сложную смесь сахаров. (Об этом, а также о других проблемах биогенеза рассказывалось в статье Пармона В. Н. Новое в теории появления жизни // Химия и жизнь. 2005. № 5.) Изучению реакции много лет мешал ее капризный характер: колбу с раствором надо было греть несколько часов без всяких видимых изменений, и вдруг в течение пары минут раствор быстро желтел, затем коричневел и загустевал. А если исходные реагенты были очень чистыми, то реакция не шла вовсе. Причиной «капризов» оказался автокаталитический характер реакции: сначала формальдегид медленно превращается в двух– и трехуглеродные сахара (гликольальдегид, глицеральдегид и дигидроксиацетон), которые затем катализируют синтез самих себя и более сложных сахаров. Если к исходной смеси добавить чуть-чуть гликольальдегида или глицеральдегида, то реакция запускается почти сразу. Другой способ ускорить ее – осветить раствор ультрафиолетом, под действием которого некоторые молекулы формальдегида соединяются в гликольальдегид. В классической реакции Бутлерова получаются сложные смеси сахаров, в которых сахара, характерные для живых клеток, перемешаны с огромным разнообразием семи-, восьми-, девятиуглеродных сахаров и даже более сложных. Если ее не останавливать вовремя, то в итоге получается коричневая карамелизованная смесь сложных сахаров и продуктов их распада. Подобная проблема часто встречается в предбиогенной химии: если к органическим веществам долго подводить энергию в виде тепла или ультрафиолета, то в итоге обычно получаются сложнейшие, неразделимые смеси веществ, похожие на смолу или деготь. Это знает на собственном опыте каждый, кому приходилось отмывать пригоревшую кастрюлю или сковородку. Чтобы получить в реакции Бутлерова именно те сахара, которые встречаются в клетках – рибозу, глюкозу, – нужно ее как-то останавливать на полпути. В последние годы было обнаружено, что некоторые минералы избирательно связывают и выводят из реакции отдельные сахара, именно те, которые нужны для биохимии. Например, при добавлении растворимых силикатов, таких как Na2SiO3 (силикатный клей), силикат-анион образует комплексы с четырех– и шестиуглеродными сахарами, которые выпадают в осадок и далее не участвуют в реакции. Так накапливаются сахара, имеющие две соседние гидроксильные группы с одной стороны: эритроза, треоза, глюкоза, манноза (подробнее об этом можно прочитать в заметке Александра Маркова на сайте «Элементы», http://elementy.ru/news/431261). Если же в реакционную смесь добавить гидроксиапатит Ca3(PO4)2 × Ca(OH)2, то на его поверхности практически избирательно осаждается рибоза (см. уже упоминавшуюся статью В. Н. Пармона в майском номере «Химии и жизни» за 2005 год)! Еще более эффективно и избирательно осаждают рибозу из реакции Бутлерова соли борной кислоты (бораты). (Ricardo et al, 2013). Соли молибдена превращают ядовитые разветвленные сахара, которые тоже получаются в реакции Бутлерова, в нужные линейные и повышают выход рибозы. Обратите внимание, что все эти вещества – силикаты, бораты, фосфаты и соли молибдена – избирательно накапливаются в грязевых котлах, которые и по другим признакам хорошо подходят на роль колыбели жизни. Получить азотистые основания оказывается проще, чем сахара. Самые разные воздействия на синильную кислоту или формамид приводят к тому, что их молекулы соединяются в кольца, такие же, как в азотистых основания. Аденин и гуанин образуются из синильной кислоты при замораживании ее водного раствора, ультрафиолетовом облучении или нагревании. Если добавить цианамид или мочевину, то получаются цитозин и урацил. Все четыре азотистых основания образуются с высоким выходом из формамида (NH2CНO) на поверхности частиц оксида титана TiO2 при ультрафиолетовом облучении; аденин, цитозин и урацил – на поверхности глины или оксидов железа при нагревании (см. обзор Constanzo et al., 2007). Получение нуклеотидов
Чтобы азотистые основания приняли участие в синтезе РНК-подобных полимеров, они должны, естественно, сначала объединиться с сахаром и фосфатом. Этот этап оказался гораздо сложнее, чем получение отдельных сахаров и азотистых оснований. Во-первых, такая реакция идет с выделением воды, и поэтому в водном растворе равновесие сдвинуто в сторону отдельных сахаров и азотистых оснований. Во-вторых, стандартные способы обхода такой проблемы – нагревание сухой смеси веществ или крепкого рассола – здесь не подходят. В этих условиях азотистые основания соединяются с рибозой, но не той стороной – связь с сахаром образует боковая аминогруппа, а не атом азота из кольца. Аденин и гуанин можно соединить с рибозой правильным способом, облучая ультрафиолетом водный раствор азотистых оснований и рибозы, но выход нужного нуклеозида не превышает 1 %, а с урацилом и цитозином этот способ вообще не работает. В клетках азотистые основания соединяются с рибозой правильно с помощью сложных ферментов, но нам надо как-то обойтись без них.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно