
|
||
|
|
||
|
|
Онлайн книга - Что за безумное стремленье! | Автор книги - Фрэнсис Крик
Cтраница 18

В случае молекулы какие-то взаимодействия существовать должны, если молекуле необходимо принять определенную конфигурацию. Было очевидно, что наилучший способ скрепления полипептидной цепи – образовать водородные связи между определенными атомами остова. Водородные связи – слабый вид связей. Их энергия лишь в десяток раз превышает энергию теплового движения молекул (при комнатной температуре), поэтому отдельная водородная связь легко рвется при постоянном тепловом возбуждении. Это одна из причин, по которым вода жидкая при нормальной температуре и давлении. Водородная связь образуется между атомом-донором (плюс атом водорода, с которым он связан) и реципиентом. В полипептидной цепи единственный сильный донор – аминогруппа NH, а единственный возможный реципиент – кислород в группе CO (карбоксильной). Джон Кендрю указал, что такая водородная связь по сути дает кольцо атомов определенного вида. Вычислив все возможные кольца такого вида, можно вычислить и все возможные структуры этого типа, каждая из которых будет определяться связью аминогруппы NH с конкретной карбоксильной группой CO, например, отстоящей на три звена в цепочке. Эта связь будет повторяться снова и снова по всей длине цепи. Образованные таким путем множественные водородные связи помогают стабилизировать структуру, защищая ее от разрушительной силы теплового движения. 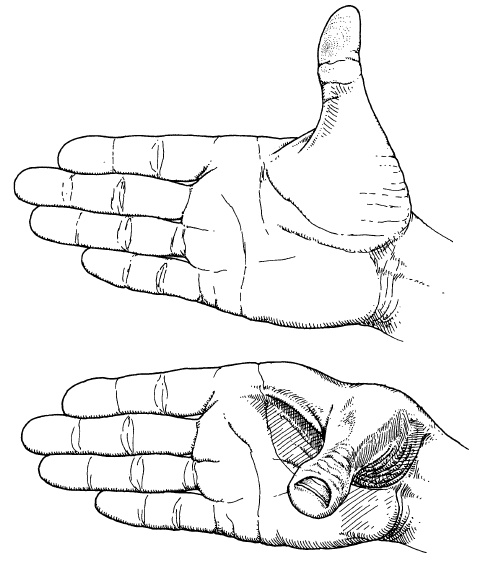
Показано, как можно поворачивать большой палец, чтобы изменить конфигурацию кисти, сохраняя все непосредственные углы и расстояния. Используя металлические модели атомов с точным соблюдением масштабов связей, Брэгг, Кендрю и Перуц пытались смоделировать все возможные варианты укладки, отбрасывая лишь те, что были недостаточно компактны. Они надеялись, что какая-нибудь из моделей лучше подойдет для объяснения данных рентгенограмм, чем прочие. На беду, они не допустили для моделей наиболее благоприятных конфигураций. Астбери показал, что рентгенограмма α-типа дает яркую точку на так называемом меридиане, с шагом, соответствующим повтору вдоль оси волокна в 5,1 ангстрем. Это указывало, что какой-то существенный элемент структуры регулярно повторяется с таким интервалом и, возможно, это расстояние между соседними изгибами. Поскольку точка наблюдалась строго на меридиане, это указывало, что винтовая ось симметрии (элемент симметрии у правильной винтовой линии) имеет целочисленное значение, хотя и нельзя было понять какое. Брэгг допускал, что ось может быть двойной, тройной, четверной, даже пятеричной и более. Как уже говорилось, у куска обоев – двумерной последовательности повторяющегося рисунка – не бывает симметрии пятого порядка, но не предвиделось причин, по которым у отдельной полипептидной спирали не может быть пятеричной винтовой оси симметрии. Это всего-навсего означает, что, если повернуть спираль на 72 градуса (360/5) и одновременно сдвинуть ее структуру вдоль оси на определенное расстояние, она останется той же самой, если пренебречь тем, что произойдет на ее концах. По этой причине Брэгг, Кендрю и Перуц строили все свои модели, исходя из целочисленных осей. Кроме того, их построения были несколько небрежны. Одну определенную группу атомов, так называемую пептидную группу, следовало в действительности рассматривать как плоскостную – все шесть ее атомов располагаются примерно в одной плоскости, – тогда как они допускали вращение вокруг пептидной связи, что делало их модели слишком вольными. Короче говоря, они сделали слишком жесткие ограничения для одного параметра (оси винтовой симметрии) и слишком мягкие – для другого (расположения пептидной связи на плоскости). Неудивительно, что все их модели выходили корявыми, и они не могли определить, какая лучше. Без особой охоты они опубликовали свои результаты в «Трудах Королевского общества», даже несмотря на их невнятность. Вышло так, что меня попросили вычитать гранки этой статьи (по-моему, гранки прислали в тот момент, когда все три соавтора отсутствовали в лаборатории), но я слишком плохо разбирался в тонкостях вопроса, чтобы понять, что именно было не так. Мои коллеги не знали о том, что Лайнус Полинг следовал тому же подходу. В настоящее время он известен широкой публике главным образом в качестве пропагандиста витамина С. В то время он был, вероятно, ведущим химиком мира. Он первым применил квантовую механику в химии (объяснив по ходу дела, например, почему валентность углерода равна четырем) и был профессором химии в Калифорнийском технологическом институте, где руководил несколькими группами очень одаренных исследователей. Его особенно интересовало применение органической химии для объяснения ключевых биологических явлений. Полинг описывает, как он впервые додумался до спирали, лежа в постели с простудой, которую схватил во время поездки в Оксфорд, куда его пригласили прочесть курс. Его основная статья об альфа-спирали вышла, наряду с рядом других его работ, в весеннем выпуске «Трудов Национальной академии наук» за 1951 г. Полинг уже знал, что пептидная связь в общем приближении плоскостная, главным образом потому, что он был более тесно знаком с органической физической химией, чем кембриджская троица. Он не пытался выстроить модель с целочисленным значением симметрии, а позволил моделям естественным образом сворачиваться в любую спираль, как им угодно. Кратность симметрии альфа-спирали оказалась равной всего 3,6 аминокислотным остаткам на один виток. Он также обратил внимание на статью Бэмборда, Хэнби и Хэппи, специалистов по полимерам, о рентгеновской дифракции на синтетическом полипептиде, где результаты вполне согласовывались с его моделью. Тот факт, что его модель не объясняла рефлекс [22] в 5,1 ангстрем на меридиане, он проигнорировал. Ирония судьбы заключалась в том, что Брэгг, Кендрю и Перуц, среди прочих моделей, сконструировали такую, которая по существу была альфа-спиралью, но они искорежили ее, бедную, чтобы добиться строго четверной кратности. Из-за этого модель выглядела слишком натянутой, да она такой и была. Вскоре стало очевидно, что альфа-спираль Полинга была верным решением. Брэгг был в унынии. Он медленно поднимался по лестнице. (Когда у Резерфорда дела шли хорошо, он прыжками взлетал по лестнице, распевая «Вперед, воители Христовы» [23].) «Величайшая ошибка в моей научной карьере», – говорил Брэгг по этому поводу. Досаду усугубляло то, что не кто иной, как Полинг решил проблему, потому что Полингу уже случалось раньше уделать Брэгга. Перуц вспомнил, что однажды после его собственного семинара местный специалист по физической химии сказал ему, что пептидная группа должна быть плоской. Перуц даже сделал письменную заметку, но так и не использовал эти сведения. Не то чтобы они вовсе не пытались получить полезный совет – просто советы, которые они получали, порой оказывались неудачными. Например, Чарльз Каулсон, химик-теоретик из Оксфорда, сказал им в моем присутствии, что атом азота может быть «пирамидальным», что оказалось весьма ошибочной информацией.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно