
|
||
|
|
||
|
|
Онлайн книга - Перспективы отбора | Автор книги - Александр Владимирович Марков , Елена Наймарк
Cтраница 41

Потомки перекормленных матерей во всех тестах продемонстрировали нарушенное социальное поведение: они не хотели общаться с сородичами и не проявляли характерного для нормальных мышей повышенного интереса к незнакомцам (рис. 22.2). 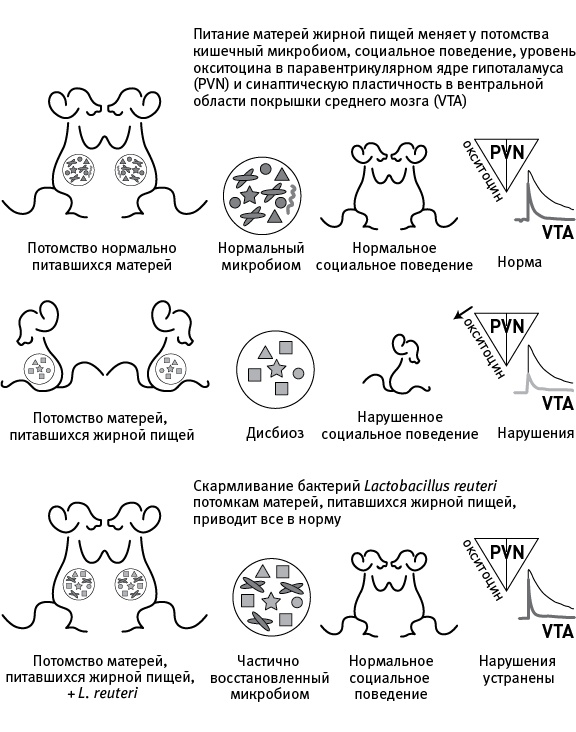
рис. 22.1. Графическое резюме исследования, продемонстрировавшего влияние кишечных бактерий на социальное поведение мышей. Потомство матерей, питавшихся жирной пищей, имеет измененную кишечную микробиоту (дисбиоз), нарушенное социальное поведение, меньшее число производящих окситоцин нейронов в гипоталамусе (PVN — паравентрикулярное ядро гипоталамуса), а также пониженную синаптическую пластичность в вентральной области покрышки среднего мозга (VTA) в ответ на социальные стимулы. Все это проходит, если искусственно заразить мышей кишечными бактериями Lactobacillus reuteri. По рисунку из Buffington et al., 2016. 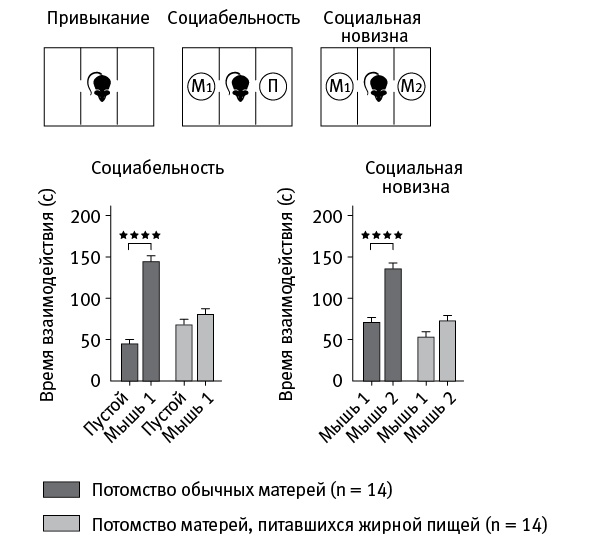
рис. 22.2. Тестирование на социабельность и интерес к незнакомцам. Тестируемую мышь сажают в камеру, подразделенную на три отсека проволочной сеткой, и дают немного освоиться (привыкание). Затем в левый отсек сажают другую мышь (M1), а правый оставляют пустым (П) — и измеряют время, проведенное тестируемым животным около каждого из двух отсеков (тест на социабельность). После этого в правый отсек сажают еще одну мышь (M2) и смотрят, привлечет ли незнакомка повышенное внимание тестируемой особи (тест на социальную новизну). По рисунку из Buffington et al., 2016. Анализ микробиоты показал, что структура бактериальных сообществ в кишечнике потомков перекормленных и нормально питавшихся матерей существенно различается, причем у их матерей эти различия примерно такие же. Теперь нужно было выяснить, существует ли связь между измененной кишечной микробиотой и нарушенным социальным поведением. Мыши практикуют копрофагию, поэтому совместное проживание с другими мышами должно способствовать обмену кишечными бактериями между особями. Оказалось, что если мышонок толстой матери поживет в одном боксе с тремя нормальными мышами 4–5 недель, то его кишечная микробиота становится почти такой же, как у обычных мышей, а социальное поведение полностью нормализуется. В качестве контроля в данном случае использовались потомки перекормленных матерей, жившие с тремя товарищами по несчастью (эти мышата так и остались социально ущербными). Таким образом, результат согласуется с предположением о том, что изменение кишечной микробиоты служит причиной нарушенного социального поведения. Следующий вопрос — какие именно изменения микробиоты ответственны за асоциальность потомства перекормленных матерей. Может быть, у них в кишечнике живут какие-то особые бактерии, нарушающие социальное поведение? Или, наоборот, у них не хватает каких-то микроорганизмов, обеспечивающих нормальное поведение здоровых мышей? Ученые проверили, что будет, если три потомка перекормленных матерей поживут несколько недель с одной нормальной мышью. Оказалось, что и в этом случае их поведение нормализуется, а нормальная мышь асоциальной не становится. Значит, дело скорее в том, что в микробиоте асоциальных мышей чего-то не хватает, а не в том, что в ней присутствует что-то вредное. Тогда мыши, полностью лишенные бактериальной микробиоты (безмикробные), тоже должны быть асоциальными. Это было проверено и подтвердилось: безмикробные мыши показали во всех тестах на социальность примерно такие же результаты, как и потомки перекормленных матерей. Каким образом кишечные микробы влияют на поведение? Может быть, у мышей с нарушенной микробиотой просто все время болит живот и поэтому им не до общения? Дальнейшие опыты, однако, показали нечто более интересное. Оказалось, что если искусственно заразить четырехнедельных безмикробных мышей микробиотой здоровых (скармливая помет), то их социальное поведение нормализуется, так же как и состав кишечных бактерий. Этого, однако, не происходит, если такую же процедуру проделать с безмикробными мышами в восьминедельном возрасте (состав кишечной микробиоты нормализуется, а социальное поведение — нет). Фекалии потомков перекормленных матерей, как и следовало ожидать, не обладают таким целительным действием, в каком бы возрасте их ни скармливали безмикробным мышам. Эти результаты показывают, что микробиота, похоже, как-то влияет на развитие мозга мышат. Метагеномный анализ выявил несколько видов кишечных бактерий, численность которых высока у контрольных мышей, но резко понижена у потомков перекормленных матерей. Сильнее всего (на порядок) сократилась численность бактерии Lactobacillus reuteri. Ранее было показано, что присутствие L. reuteri влияет на выработку окситоцина (Poutahidis et al., 2013). Таким образом, начал прорисовываться возможный механизм влияния микробиоты на социальное поведение: жирная диета снижает численность L. reuteri у матерей и их потомства, что ведет к снижению производства окситоцина в мозге и, как следствие, к асоциальности. Чтобы проверить эту гипотезу, ученые добавляли живых бактерий L. reuteri в воду, которой поили потомство перекормленных матерей в возрасте от 3 до 7 недель. В соответствии с ожиданиями, эта «биодобавка» нормализовала социальное поведение подопытных животных. На обычных мышей она не повлияла — очевидно, потому что у них и так есть достаточное количество L. reuteri в кишечнике. Мертвые бактерии L. reuteri от асоциальности не излечивают. Неэффективным оказалось и добавление в воду другого вида того же рода, L. johnsonii, численность которого тоже понижена у потомков перекормленных матерей. У потомства матерей, страдавших ожирением, и у безмикробных мышей, помимо асоциальности, наблюдаются и другие симптомы, характерные для аутизма: повторяющиеся действия и повышенная тревожность. Эти симптомы не исчезают ни от добавления L. reuteri в воду, ни от скармливания мышатам помета обычных мышей. Правда, ранее было показано, что они снимаются добавлением в пищу человеческой кишечной бактерии B. fragilis. Так или иначе, влияние L. reuteri весьма специфично: оно затрагивает только социальное поведение, но не другие признаки расстройств аутистического спектра, характерные для мышей с нарушенной кишечной микробиотой. В полном соответствии с гипотезой, согласно которой L. reuteri влияет на социальное поведение через активацию окситоциновой системы мозга, у потомства перекормленных матерей в паравентрикулярном ядре гипоталамуса, отвечающем за производство окситоцина, оказалось пониженным число нейронов, производящих этот самый окситоцин (при неизменном общем числе нейронов в этом ядре). Добавление L. reuteri в питьевую воду нормализует количество выделяющих окситоцин нейронов (рис. 22.1). Важнейшую роль в социальном поведении млекопитающих играет система внутреннего подкрепления, фундамент которой составляют дофаминовые нейроны вентральной области покрышки среднего мозга (VTA, Ventral Tegmental Area). Эти нейроны получают окситоциновые сигналы из паравентрикулярного ядра, что повышает их восприимчивость к другим сигналам (глутаматэргическим), несущим социально значимую информацию. Попросту говоря, от окситоцина, приходящего в VTA из паравентрикулярного ядра, зависит интерес к сородичам и удовольствие, получаемое от общения с ними.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно