
|
||
|
|
||
|
|
Онлайн книга - Эволюция Вселенной и происхождение жизни | Автор книги - Пекка Теерикорпи
Cтраница 127

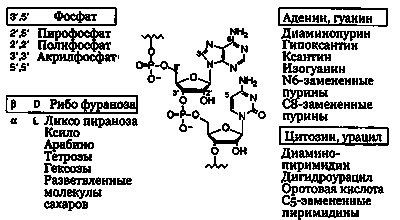
Теперь расскажем о проблемах полимеризации. На рис. 30.5 показаны формы субъединиц нуклеозидов и их фосфодиэфирные связи в РНК-полимерах. На этом рисунке изображены и альтернативные строительные блоки, которые не могут быть использованы в РНК-полимерах. Как уже говорилось, РНК-нуклеотиды формируются из оснований — аденина, гуанина, цитозина и урацила, соединенных с сахаром рибозой (см. рис. 28.4 и 28.5). Соседние сахара рибозы должны связываться друг с другом через фосфоризирующие связи между 5'-углеродом одной рибозы с 3'-углеродом предыдущей. Фосфоризирующая связь формируется через фосфатную часть, содержащую фосфор (Р) и кислород (О). Для этого нуклеозиды должны сначала связать фосфатную группу (см. рис. 28.4) или фосфоризироваться своим 5'-углеродом, чтобы затем превратиться в нуклеотиды. На молодой Земле это было затруднительно, так как растворимых фосфатов почти не имелось. Возможно, небольшая часть фосфатов образовалась из неорганических минералов фосфата кальция (гидроксилапатит), хотя они очень плохо растворяются в воде. Возможно также, что фосфаты появились из линейных полифосфатов вулканического происхождения или продуктов их распада. Даже если эти источники обеспечивали нужное количество растворимых фосфатов, то фосфоризация нуклеозидов должна была быть очень затруднена, ведь в лабораторных условиях она может быть завершена только при наличии мочевины, хлористого аммония и тепла. Далее, для полимеризации нуклеотидов нужно еще, чтобы они были активированы какой-нибудь высокоэнергичной связью (например, связью с аналогом основания или аминокислотой) в положении 5', чтобы обеспечить энергией реакции связи между нуклеотидами.
Рис. 30.5. Полимеры, сформированные фосфодиэфирными связями (содержащими фосфор и кислород) между 5'- и 3'-углеродами β-D-нуклеотидов. Нуклеозиды образованы из оснований аденина, гуанина цитозина, урацила и четырехуглеродной циклической формы рибозы в D-ориентации. Перепечатано с разрешения Macmillan Publishers Ltd; G. F. Joyce: The Antiquity ofRNAbased evolution. Nature 418:214, copyright (2002). Еще одна трудность полимеризации рибонуклеотидов состоит в том, что в смеси мономеров могут происходить различные реакции. Чтобы сформировать функциональный полимер, фосфоризирующие соединения должны образовываться между 5'- и 3'-углеродами соседних нуклеотидов. Но кольцо рибозы имеет реакционноспособные группы ОН у углеродов в положениях 5', 3' и 2. В добиологических условиях между всеми этими группами могли протекать реакции, и в результате внутримолекулярных реакций между ОН-группами в положениях 2' и 3' могли формироваться циклические соединения. Более того, молекулы фосфатов могли создать разные полифосфатные связи между разными углеродами. Все эти разнообразные связи могли привести в тупик дальнейшую полимеризацию. По мнению Джеральда Джойса (Исследовательский институт Скрипса, Ла-Хойя, Калифорния), ведущего специалиста по добиологической химии РНК, отсутствие специфичности является основной проблемой добиологических реакций. Спонтанные реакции, начавшиеся с синильной кислоты или с цианистого ацетилена, цианита и мочевины, могут дать разные аналоги оснований. Но из всех них только пурины аденин и гуанин, а также пиримидины цитозин и урацил природа использовала для формирования функциональных нуклеозидов. В составе нуклеозидов в добиологических условиях существующие основания могли быть связаны с составляющими рибозы, причем с одинаковым успехом как в а-, так и в р-конфигурациях, а фураноза (четырехуглеродное кольцо) рибозы могла сформироваться как в L-, так и в D-изоформах (лево- и правовращающих плоскость поляризации света, как описано в главе 28). Сахар рибоза также мог сформироваться в виде пятиуглеродного кольца (пираноза) путем соединения 5'- и 1'-углеродов. Добиологические реакции полимеризации между всеми различными аналогами и изоформами нуклеотидов могли привести к большому разнообразию фосфатных соединений разных атомов углерода рибозы. В целом эти реакции могли легко использовать разные варианты пуринов и пиримидинов, связываясь с которыми разные производные разных циклических сахаров формируют L- и D-конфигурации. Эти совершенно случайные аналоги нуклеозидов могут затем фосфорилироваться на разных позициях углерода, и потом опять случайно фосфорилированные аналоги нуклеотидов могли связаться друг с другом разными способами, что показано на рис. 30.5. Ни один из этих альтернативных вариантов не производит функциональноактивные РНК-полимеры. Только правильно сформированные и полимеризированные нуклеотиды могут быть функциональными шаблонами для репликации через комплементарное спаривание оснований. Мы не понимаем, как жизнь при отсутствии каких-либо ферментных реакций отбора выбирала как раз нужные нуклеотидные компоненты и их специфические изоформы и как она контролировала формирование фосфоризующих связей только между 5'- и 3'-углеродами нуклеотидов. Следующей проблемой при сборке длинных РНК-полимеров является их врожденная неустойчивость. РНК-полимеры легко делятся на части гидролизом, и их функциональная последовательность может быть утрачена из-за многочисленных ошибок копирования или мутаций. При рассмотрении всех этих химических обстоятельств кажется, что полный каскад реакций для формирования функциональных полинуклеотидов (включая синтез нуклеозидных оснований и рибозы, сборку нуклеозидов, их фосфорилирование и активацию и, наконец, полимеризацию и стабилизацию полимеров) был трудноосуществим в добиологических условиях. Эти процессы выглядят настолько непохожими, что возникло предположение, что РНК-миру предшествовали какие-то другие механизмы хранения и переноса информации, которые затем «управляли» (или обеспечивали катализаторами) миром РНК-оснований. Но трудно объяснить, как мог произойти переход от более примитивной генетической системы к РНК. Разумеется, можно предположить, что мы пока еще не нашли таких условий, химических способов и факторов отбора, которые могли бы сделать возможной добиологическую химию и эволюцию. Новый многообещающий способ добиологического синтеза нуклеотидов — прямо из формамида — сейчас исследуется в лабораториях Р. Саладино (R. Saladino) и Э. Димауро (E.DiMauro) в университетах Тусции и Рима (Италия). Формирование генетического кода. Хотя молекулы РНК могут стимулировать некоторые типы химических реакций, теперь мы знаем, что белковые катализаторы значительно превосходят их по универсальности и эффективности. Поэтому изобретение генетически закодированного синтеза белков дает огромное преимущество для развития жизни. Это делает возможным появление и эволюцию основанных на ДНК геномов, сложных клеточных структур и современных биохимических процессов жизни. Рождение синтеза белков было настолько важным для эволюции жизни, что Энтони Пул (A. Poole) и его коллеги из Стокгольмского университета (Швеция) назвали существо, у которого появился этот механизм, прорывным организмом, или Riborgis eigensis. Но возникновение генетически закодированного синтеза белков должно было «случайно» — или совершенно неожиданно — изменить химическую эволюцию на базе РНК. В самом деле, невозможно предвидеть какие-либо эволюционные «изобретения» до момента их неожиданного появления. Как мы знаем, для синтеза белков нужен сложный аппарат, состоящий из каталитических рибосомных комплексов (чтобы считывать генетический код и формировать пептидные связи), тРНК и аминёкислот, а еще требуются катализаторы, связывающие аминокислоты с тРНК (см. главу 28). Важнейшие компоненты этого механизма формируются молекулами РНК. Поскольку обе центральные каталитические функции, вовлеченные в процесс трансляции (аминоацилирование тРНК и формирование пептидных связей), могут управляться РНК-ферментами, то возможно, что исходная форма этого аппарата была создана РНК-миром. Но такие сложные механизмы не возникают вдруг, случайно; они должны развиваться, постепенно эволюционировать из некоторых ранее существовавших функций. Раз синтеза белков до этого не существовало, значит, исходный аппарат трансляции должен был развиться из чего-то другого. Группа Дэйвида Пенни из университета Массей (Новая Зеландия) предположила, что исходной функцией этого молекулярного механизма была репликация РНК и что все компоненты более позднего трансляционного аппарата клетки (проторибосомы, прото-тРНК и аминокислоты) были уже вовлечены в эту функцию. Организуя ранние функции этих компонентов, можно облегчить переход от их исходного взаимодействия к развитию процесса трансляции.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно