
|
||
|
|
||
|
|
Онлайн книга - Жизнь замечательных веществ | Автор книги - Аркадий Курамшин
Cтраница 5

1. Вещества, которые принято считать «неживыми»
В начале XIX века Йёнс Якоб Берцелиус разделил существующую в те времена химию на «органическую», которую он и его последователи рассматривали как «химию живых организмов», и «неорганическую» – «химию неживого». Хоте уже через 20 лет после такого размежевания Фридрих Вёлер (случайно, правда) показал, что границы между «химией живого» и «химией неживого» нет, а в 1850-х годах Эдуард Франкланд добавил третий раздел химии – «металлоорганическую», для большинства людей, представление которых о химии ограничивается курсом средней общеобразовательной школы, в памяти сохраняется это противостояние живого и неживого, ведь как иначе можно объяснить то, что на полном серьёзе появляется термин «органические продукты питания», ведь из того, что мы едим или пьём, «неорганическими» являются только поваренная соль и вода. Вместе с тем, как учит диалектика, противоположности не только борются друг с другом, но и находятся в единстве. Точно так же многие неорганические вещества важны для нормальной работы живых систем, а некоторые образуются в результате их жизнедеятельности, и, конечно же, каждое по-своему замечательно. 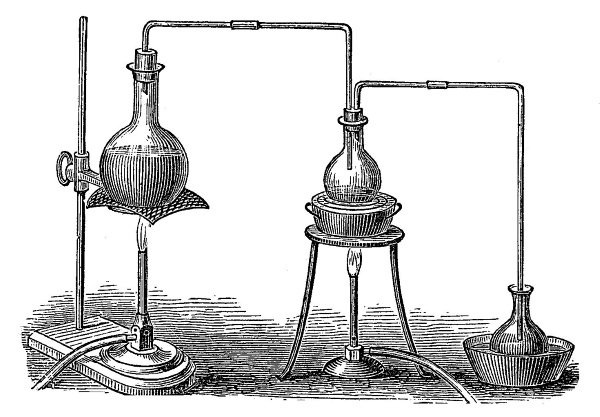
1.1. Соляная кислота

Подавляющая часть людей, отсидев на уроках химии в школе, сохраняет в памяти названия четырех кислот – азотной, серной, соляной и уксусной. При этом большинство если и догадываются, что уксусную кислоту мы можем найти на кухонной полке в виде раствора уксуса для консервирования или готовки, серную – в аккумуляторе автомобиля, то насчёт азотной и соляной кислот уж точно уверены, что с ними они попрощались, выйдя за ворота школы. Однако я гарантирую вам, что соляная кислота сопровождает вас с самого рождения и является неотъемлемой частью вашей жизни – она играет существенную роль в процессах, протекающих в организме. Эта сильная кислота, водный раствор хлороводорода в воде, была известна очень давно. Ранние названия этого замечательного вещества были связаны с её запахом, который, как казалось алхимикам, связан с морской свежестью (из чего я делаю вывод, что либо они нюхали какое-то не то море, либо не обжигали хлороводородом слизистые носоглотки), а также с тем, что эту кислоту получали из морской (каменной, поваренной) соли. В алхимических трактатах хлороводород упоминается как «дух соли» или «соляной спирт» (spiritus salis), потом появился термин «муриевая кислота» (muria – рассол, соленая вода). Термином «muria» называлось особо едко-соленое ощущение. В одном из трактатов XVII века можно встретить разъяснение: «Muria – это едко-соленое». 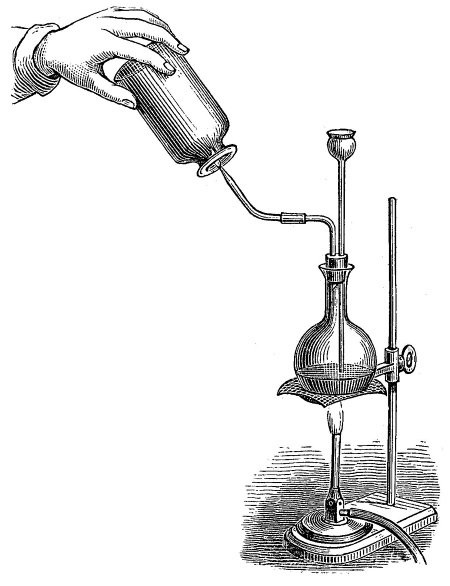
Кстати, становление номенклатуры в России проходило через причудливые этапы, одним из которых была попытка пойти своим собственным путем и русифицировать все названия. Так, в одной из российских рукописей, относящихся к 1870 году, можно прочитать: «Водород хлорович взаимодействует с глиноземием с образованием глиноземия хлоровича». В 1870–1875 гг. в Петербургской академии наук обсуждалась возможность использования для названий химических веществ таких сочетаний слов, которые напоминали бы русские фамилии и отчества. Например, для воды Н2О предлагалось название «водород кислородович», для хлорида калия КСl – «калий хлорович» или «потассий хлорович», для хлороводорода НСl – «водород хлорович», для гипохлорита калия КСlO – «калий хлорович кислов», для хлората калия КСlO3 – «калий хлорович трёхкислов» и т. п. В приведенной цитате говорилось о взаимодействии алюминия («глиноземия») с раствором хлороводорода в воде – соляной кислотой HCI: 2Al + 6НСl = 2АlСl3 + ЗН2. Точная дата первого получения соляной кислоты неизвестна. Алхимики могли получать смеси, содержащие соляную кислоту, практически с самого начала алхимических изысканий. Существует предположение, что первым соляную кислоту получил в начале IX века Джабир ибн Хайян – знаменитый арабский алхимик, врач, фармацевт, математик и астроном, которому также приписывается открытие мышьяка, сурьмы и висмута. Естественно, соляная кислота в Cредневековье применялась при изготовлении царской водки (смеси соляной и азотной кислот). Известно, что чистый газообразный хлороводород был впервые получен Джозефом Пристли в 1772 году, а в 1818 году Хэмпфри Дэви успешно доказал, что полученный газ состоит из хлора и водорода. Первоначально хлороводород, образующийся попутно при переработке каменной соли и получении соды, был отходом промышленного производства, просто стравливавшимся в воздух. Однако в середине XIX века такой подход и загрязнение окружающей среды стали рассматриваться как неприемлемое решение. К счастью, к тому же самому времени газообразный хлороводород стал применяться как ценный источник для производства соляной кислоты. Несмотря на то что подходы с тех времен значительно изменились, соляная кислота до сих пор получается как продукт утилизации отходов производства. Правда, сейчас большую часть соляной кислоты получают, утилизируя хлороводород, выделяющийся при хлорировании органических соединений. 
При этом хлороводород очень часто применяют для получения хлорорганических соединений. Например, в результате присоединения хлороводорода к тройной связи ацетилена образуется хлорвинил, из которого с помощью полимеризации получают полихлорвинил (ПВХ) – материал, применяющийся для электроизоляции проводов и кабелей, производства листов, труб (преимущественно хлорированный поливинилхлорид), плёнок, плёнок для натяжных потолков, искусственных кож, поливинилхлоридного волокна, пенополивинилхлорида, линолеума, обувных пластикатов, мебельной кромки и т. д. 
Поскольку хлороводород образуется в качестве побочного продукта производств органических соединений и используется в промышленном производстве органических соединений, чаще всего хлороводород эффективно получают и употребляют в рамках одного и того же производства, что выгоднее выделения отдельного производства хлороводорода и логистики по его доставке потребителю. Ещё одним способом масштабного промышленного применения раствора хлороводорода – соляной кислоты – является травление металлических поверхностей. Хотя соляная кислота играет определенную роль в пищевой промышленности (корректировка кислотного уровня воды, применяющейся при приготовлении пищи), гораздо более существенную роль она играет в потреблении пищи. В нашем желудке содержится порядочное количество соляной кислоты, а рН желудочного сока может достигать единицы (это соответствует раствору с примерным содержанием кислоты 0,35 %). |
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно