
|
||
|
|
||
|
|
Онлайн книга - Неалкогольная жировая болезнь печени | Автор книги - Е. Вовк
Cтраница 10

Рис. 25. Стеатоз печени Содержание ТГ в печени при НАЖБП, как вне- так и внутриклеточно, может достигать 40 % от массы органа (при норме около 5 %). Вначале жир накапливается в цитоплазме гепатоцитов и оттесняет ядро к периферии клетки (рис. 26). По мере накопления ТГ некоторые гепатоциты разрываются и образуются внеклеточно расположенные жировые кисты. Деструкция гепатоцитов является причиной первичной миграции лейкоцитов: сначала нейтрофилов и макрофагов, а затем и лимфоцитов, и запуска хронического воспаления, которое становится важнейшим независимым фактором прогрессирования НАЖБП до НАСГ и фиброза печени. 
Рис. 26. Смешанный стеатоз печени преимущественно в 3-й зоне ацинуса в сочетании с небольшим количеством телец Маллори (окраска гематоксилиномэозином, х200) В формировании НАСГ выделяют несколько основных патогенетических механизмов, так называемых ударов или толчков (hits). При ожирении в роли «первого толчка» выступает первичное накопление свободных жирных кислот и триглицеридов в гепатоците. Печень становится местом накопления триглицеридов, которые синтезирует из алиментарных жирных кислот или углеводов — глюкозы и фруктозы [20]. При инсулинорезистентности и сахарном диабете источником поступления в печень жирных кислот служит липолиз, и ТГ поступают из жировой клетчатки [21]. В отсутствии ожирения при пищевой перегрузке готовыми или вновь синтезированными из углеводов жирными кислотами нейтральный жир накапливается в подкожной бурой жировой клетчатке как запасной энергоноситель. Эктопическое отложение жира (в печени, поджелудочной железе, миокарде и скелетных мышцах) происходит после «перегрузки» жировой ткани циркулирующими в крови триглицеридами. Иначе говоря, печень становится дополнительным местом складирования триглицеридов и, как бурая жировая ткань, становится резервуаром энергетических субстратов — в гепатоцитах развивается микровезикулярный стеатоз [22]. Само по себе избыточное накопление ТГ как в жировой ткани, так и эктопическое всегда сопровождается повреждением какой-то части гипертрофированных клеток (адипоцитов, гепатоцитов или кардиломиоцитов) — к ним мигрируют активированные макрофаги, которые в результате фагоцитоза выделяют цитокины и первично активируют иммунные реакции замедленного типа — развивается хроническое системное воспаление. Среди выделяемых жировой тканью перилипинов особое значение для патогеназа НАЖБП имеет снижение секреции адипонектина и увеличение секреции лептина, что приводит к потере контроля над чувством насыщения (рис. 27). 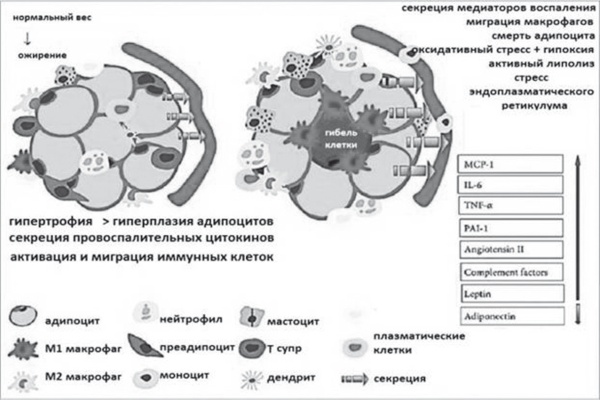
Рис. 27. Провоспалительная активность адипоцитов при НАЖБП (модифицировано по Wang W. et al., 2014) [23] Перегруженная жиром ткань становится инсулинорезистентной, поскольку стремится ограничить дальнейший синтез триглицеридов, в гепатоцитах развивается макровезикулярный стеатоз, и жир начинает накапливаться внеклеточно. Инсулинорезистенность — снижение реакции на инсулин чувствительных к инсулину тканей при его достаточной концентрации. Основные органы-мишени инсулинорезистентности: скелетные мышцы, жировая ткань, печень, мозг. Фактически печень принимает функции белой жировой ткани — синтезирует провоспалительные и прогипергликемические перилипины, что углубляет инсулинорезистенность. Сегодня известно, что инсулинорезистентность имеет полигенный характер. В ее развитии участвуют мутации генов субстрата инсулинового рецептора (СИР-1), гликоген-синтетазы, гормон-чувствительной липазы, b3-адренорецепторов, фактора некроза опухолей-α (ФНО-а), разобщающего протеина (UCP-1), а также молекулярные дефекты белков, передающих сигналы инсулина (увеличение экспрессии Rad-белка и UPC-1 ингибитора тирозин-киназы инсулинового рецептора в мышечной ткани, снижение мембранной концентрации и активности внутриклеточных транспортеров глюкозы GLUT-4 в мышечной ткани). Остается неясным вопрос — какие механизмы у каждого конкретного пациента на тканевом и системном уровне настраивают этот предел ожирения, при превышении которого развивается инсулинорезистентность и, как следствие, гиперинсулинемия с дальнейшим набором веса и перспективой сахарного диабета 2 типа. Фактически, достаточно много людей остаются метаболически «здоровыми» даже при тяжелом ожирении [24]. При прогрессировании MC и развитии инсулинорезистентности печень, в норме не участвующая в депонировании избыточного жира, начинает еще более активно аккумулировать ТГ, поступившие в кровь вследствие липолиза, и активно синтезирует СЖК и ТГ из избытка глюкозы в плазме. Инсулинорезистентность приводит к развитию компенсаторной гиперинсулинемии и одновременно «переводит» обмен веществ с окисления глюкозы на b-окисление жира. Не только в мышечной ткани, но и в печени, и в мозге свободные жирные кислоты конкурируют с глюкозой как основным энергетическим субстратом — этот путь получения энергии всегда сопряжен с развитием феномена липотоксичности. Липотоксичность — «второй толчок» в патогенезе НАЖБП и главная причина развитии НАСГ. Развивается как следствие оксидативного стресса гепатоцитов при активации в них липолиза и напряженном синтезе жирных кислот, которые происходят в митохондриях и эндоплазматическом ретикулуме. Липотоксичность приводит к появлению в гепатоцитах и системно большого количества свободных перекисей и перекисному окислению липидов (ПОЛ), при котором активно повреждаются ПНЖК фосфолипидов клеточных мембран: цитоплазматической мембраны клетки и главное — мембран, из которых состоят сами митохондрии и эндоплазматический ретикулум [25–27]. 
Рис. 28. Основные этапы патогенеза НАЖБП Разрушение ПНЖК фосфолипидов нарушает структуру, метаболическую активность и сигнальную функцию клеточных мембран. Перекиси также опасны для ДНК и РНК гепатоцитов. Липотоксичность запускает апоптоз гепатоцитов, приводит к НАСГ — в паренхиме печени на фоне жировой инфильтрации развивается первично хроническое воспаление и фиброз, а также формирует воспалительный статус плазмы [28]. Таким образом, НАСГ обладает внутренним потенциалом к прогрессированию и приводит к развитию более или менее выраженного фиброза печени у каждого пациента и находится в фокусе научных исследований [12,13]. Глава 7
НАЖБП как предиктор ССЗ В общей медицинской практике НАЖБП и особенно НАСГ рассматриваются как мульсистемное заболевание, в связи с его ролью в атерогенезе и формировании кардио-метаболического континуума [29]. Действительно, в глобальном масштабе социально-значимым при НАСГ является увеличение риска развития сахарного диабета 2 типа, ССЗ, хронической болезни почек, а также рака печени и толстой кишки [30]. НАСГ в 6-10 раз увеличивает риск смерти от цирроза и рака печени и в 5 раз — риск смерти от ССЗ, вне зависимости от всех других предикторов кардиоваскулярной патологии [3, 7]. Marchesini G. et al. (2003) в относительно «ранней» работе показали, что у пациентов без диабета и с гистологически верифицированной формой НАЖБП метаболический синдром на 35 % чаще встречается при НАСГ, чем при простом стеатозе печени (рис. 29). Авторы показали, что тяжесть НАСГ вне зависимости от пола, возраста и степени ожирения тесно коррелирует со степенью фиброза печени (OR, 3.5; 95 % CI, 1.1-11.2; P =.032) и тяжестью MC, которую маркирует инсулинорезистентность (ИР) (OR, 3.2; 95 % CI, 1.2–8.9; P =.026) [31]. |
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно