
|
||
|
|
||
|
|
Онлайн книга - История лазера | Автор книги - Марио Бертолотти
Cтраница 14

Длины волн излучения, которое испускается веществом, может также и поглощаться им на тех длинах волн. Если, например, мы посылаем интенсивный свет, содержащий все видимые длины волн (непрерывный спектр излучения), через пламя в котором сгорает натрий, то в пропущенном свете обнаружится отсутствие длин волн, соответствующих двум желтым линиям D-линии натрия. В спектре две темные линии появляются в тех местах, в которых наблюдаются две яркие линии в спектре излучения. Это объяснение применимо не только для нашего Солнца, но и для любой звезды. Действительно, темные линии, подобные тем, что Фраунгофер наблюдал в солнечном спектре, наблюдаются и в спектрах звезд, и положение этих линий указывает, какие длины волн поглощаются веществами в звездных атмосферах, что позволяет определить эти вещества. 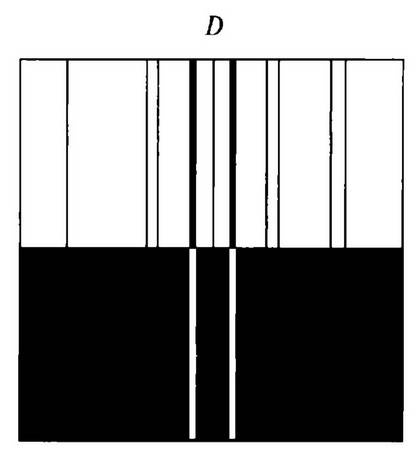
Рис. 10. Обращенные линии. На верхней части показаны D-линии натрия (дублет), которые проявляются как черные линии в солнечном спектре. На нижней части показаны яркие D-линии натрия, которые получаются в лаборатории в парах пламени Фундаментальные открытия новой науки спектроскопии были сделаны Кирхгофом, Брюстером, Дж. Гершелем (1792—1871), Тальботом, Чарльзом Уитстоном (1802—1875), А. Ангстремом (1814—1874) и Вильямом Сваном. Тот факт, что спектры веществ иногда состоят из набора дискретных линий, а иногда представляют полосы, был, наконец, после многих дискуссий, объяснен Джорджем Сале (1875) путем сопоставления линейчатых спектров с атомами, а спектров полос — с молекулами. Атомы
Уже Демокрит и Лесипс в V в. до н.э. говорили об атомах. Римский поэт Лукреций (98—55 до н.э.) в De rerum natura, объясняя теорию Демокрита, говорил, что воздух, земля и все другие вещи мира сделаны из набора частиц или корпускул — атомов, находящихся в безостановочном и очень быстром движении, которые столь малы, что не видимы человеческим глазом. Атомы предполагались быть крайним результатом последовательного разделения вещества на все меньшие части. Слово «атом» по-гречески означает «неделимый». Однако идеи Демокрита и Лукреция далеки от нашего понимания атомов, поскольку они не рассматривали существования многих сортов атомов и того, что атомы определенного вещества одинаковы. Выраженная смутным и неконкретным образом атомистическая теория Демокрита теряла свое значение, и слово «атом» стало употребляться для обозначения объекта крайне малого размера. Лукреций имел успех совсем в другой области, высказав гипотезу, что заразные болезни распространяются очень малыми частицами. В эпоху Возрождения итальянский философ и врач Джироламо Фракасторо (1483—1553) возродил эту теорию. Однако эта идея бактериологии оставалась секретом, пока Луи Пастер (1822—1895) вновь не обратился к ней. Во всяком случае, атомистическая гипотеза Демокрита и Лесипса была принята священником Гассенди (1592—1655), который активно провозглашал, что даже если эта гипотеза находит подтверждение у «развратных» Эпикура и Лукреция, но она не имеет прямой связи с религиозными философиями их античных последователей — и может быть принята христианами. Идеи Гассенди оказали глубокое влияние на химика Роберта Бойля, которому мы обязаны обозначениями химических элементов. Эти обозначения стали более точными, когда А.-Л. Лавуазье (1743—1794) открыл, что определенные химические соединения содержат элементы в определенных пропорциях и что масса веществ остается постоянной до и после протекания химической реакции. Эти исследования получили завершение в работе Джона Дальтона (1766—1844), который изложил их в своей книге A New System of Chemical Philosophy (опубликованной в Манчестере в 1808 г.) концепцию, что существует много сортов атомов, каждый из которых характеризует разные вещества и что атомы в определенном веществе идентичны. Дальтон доказал, что каждому химическому элементу можно приписать число, которое представляет вес одного атома данного элемента. Атомный вес
В настоящее время атомный или молекулярный вес измеряется сравнением веса атома данного вещества с атомом водорода. Вес атома водорода удобно считать приблизительно одной единицей атомной массы (вес одной атомной массы 1,66∙10—24 г), так, вес атома углерода 12. Атомный вес кислорода почти 16 (точно 15,9994) и поскольку молекула кислорода состоит из двух атомов, один моль молекулы кислорода весит около 32 г. Из определения моля следует, что моль всегда содержит одно и то же число атомов и молекул (так, называемое число Авагадро NА = 6,022∙1022). Однако существование атомов все еще было спорным, поскольку никто не мог сказать, что видел их, и в ходу были различные идеи. В 1860 г. на Химическом конгрессе в Карлсруе, первом международном собрании, участники продолжительно обсуждали различия между атомами и молекулами и не пришли к определенному заключению. Сегодня мы определяем молекулу как химическую комбинацию двух или более идентичных или различных атомов, которая может стабильно существовать и которая представляет наименьшее количество вещества и обладает характеристическими свойствами данного вещества. Электрон появляется
В то время, как развивались атомные и молекулярные теории в химии, в исследованиях в области электрической проводимости в жидкостях и электрических разрядов в газах при низком давлении обнаружилось, что атом вовсе не «неделимый», но содержит в себе электрические заряды. Г. Дж. Стони (1826—1911) в 1874 г., пытаясь простым способом объяснить законы электролиза, установленные Фарадеем в 1833 г., ввел «атом» электричества, который он позднее (1891 г.) назвал «электроном». До этого Г. Гельмгольц (1821 — 1894) говорил: «Если мы принимаем гипотезу, что элементарные субстанции состоят из атомов, мы не можем избежать заключения, что электричество также, положительное и отрицательное, разделяется на элементарные порции, которые ведут себя подобно атомам электричества». Таким образом, умозрительный электрон допускался только как свойство, относящееся к электрическому разряду. Однако английский физик Дж. Дж. Томсон (1856—1940) открыл в 1897 г., что в электрических разрядах в газах присутствуют очень маленькие частицы с отрицательным зарядом, которые испускаются атомами. Томсон измерил их удельный заряд (e/m), т.е. отношение заряда к массе. Поскольку атом сам по себе нейтрален, открытие электрона — за это Томсон в 1906 г. получил Нобелевскую премию по физике — означает, что атом должен включать в себя как отрицательные заряды (электроны), так и положительные заряды. Нобелевская премия
Поскольку многие из упоминаемых здесь исследователей были удостоены этой престижной премии, уместно несколько отвлечься, и сообщить, как она возникла и как присуждается. 10 декабря 1896 г. шведский химик Альфред Нобель скончался в возрасте 63 лет, в своем доме в Сан Ремо. Он сделал возможным практическое применение нитроглицерина, создав динамит. Нитроглицерин был синтезирован в 1846 г. А. Собреро (1812—1888), а Альфред Нобель применил для его стабилизации некоторые инертные вещества. В результате в 1875 г. был получен первый динамит, представляющий собой желатинообразную смесь нитроглицерина с клетчаткой. В 1889 г., смешивая в различных пропорциях коллоидную клетчатку с нитроглицерином, он сумел создать баллистит, который до сих пор используется, как бездымное взрывчатое вещество. Изготавливался динамит на фабрике вблизи г. Турина (Италия). Благодаря своим патентам, а также эксплуатации нефтяных месторождений в Баку, Нобель стал обладателем огромного состояния, исчислявшимся на современные деньги в несколько сотен миллионов евро. Это состояние, желая сгладить возможное разрушительное использование людьми его изобретений, он завещал использовать как фонд для премий. Уместно процитировать отрывок из его завещания:
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно