
|
||
|
|
||
|
|
Онлайн книга - Кишечник долгожителя. 7 принципов диеты, замедляющей старение | Автор книги - Алексей Москалев
Cтраница 19

Таблица 21. Нутриенты и долголетие 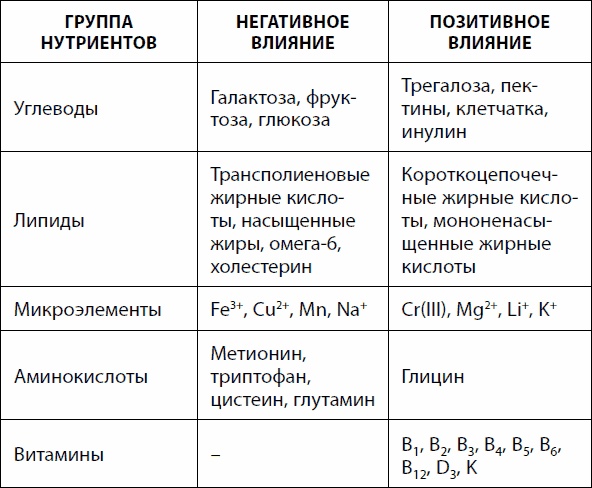
В любой момент, в зависимости от полученных извне инструкций или внутреннего состояния, клетка делает выбор между несколькими стратегиями существования. Если в нее поступает достаточное количество питательных веществ или она стимулируется особыми сигнальными молекулами – факторами роста, то клетка растет и, в зависимости от типа ткани, делится. Когда клетка голодна, находится в стрессе (высокая температура, кислородное голодание) или не получает гормональной стимуляции, она выходит из программы роста, прекращает деления. При этом она занимает выжидательную позицию, включая дополнительную защиту от стресса и пытаясь пережить неблагоприятный период. Если стрессовые условия не прекращаются, истощаются защитные механизмы или клетка сильно повреждена изнутри, она либо навсегда выходит из клеточного цикла, при этом теряет способность к делениям (клеточное старение), либо самоликвидируется (запрограммированная гибель клетки, или апоптоз). Где же тут механизмы старения? Когда клетке хорошо, она растет и затем делится, а затратные процессы поддержания устойчивости к стрессам выключаются за ненадобностью. В этот момент ошибки и поломки начинают накапливаться, ускоряя старение. Сам по себе стресс тоже приводит к накоплению поломок. Если стресс сильный, клетка ускоренно старится или погибает. Однако когда клетка лишь периодически голодает или подвергается очень умеренным стрессам, она включает защиту, которая не только устраняет те ошибки, что возникли, но и переводит всю систему на более высокий уровень устойчивости к последующим стрессам и поломкам. Именно поэтому прерывистое голодание, ограничительная диета или периодическое стресс-воздействие (температурное закаливание, гипоксическая тренировка, аэробные физические нагрузки) замедляют старение и продлевают жизнь. Переключение между стратегиями существования клетки контролируется особыми регуляторными белками. В настоящий момент известно около десятка таких ключевых белков, о некоторых я расскажу. Хорошей новостью является то, что нам известны вещества, которые содержатся в продуктах питания и способны влиять на активность переключателей клеточных программ, а значит, вероятнее всего, и на скорость нашего старения. Как работает переключатель? Клетка состоит из оболочки (мембраны), цитоплазмы (жидкого внутреннего содержимого, в котором плавают структурные составляющие клетки – митохондрии, лизосомы и др.) и ядра (в нем функционируют хромосомы, несущие генетические инструкции). С одной стороны, клетка получает сигналы от факторов роста (рис. 4). Для того чтобы их воспринимать, она вооружена особыми «приемниками» – белками-рецепторами. Как правило, такие «антенны» расположены на поверхности клетки. Если же сигнал – жирорастворимая молекула (стероидный гормон, витамин D, гормоны щитовидной железы), то она проникает через жировую оболочку клетки, и поэтому приемники находятся прямо в ядре. Сигнал от рецептора передается через каскад последовательно активируемых белков, основную часть из которых составляют различные киназы. Заканчивается передача сигнала на транскрипционных факторах. Последние представляют собой белки, которые способны активировать считывание генетических инструкций в клеточном ядре, активируя синтез нужных клетке белков. Все довольно элегантно устроено – взаимодействуя между собой, одни клетки через факторы роста управляют функциями других. С другой стороны, клетка измеряет количество поступающих питательных веществ, прежде всего аминокислот, уровень свободных радикалов, повреждений белков под действием температуры, повреждений ДНК под влиянием мутагенов, ионизирующей радиации или ультрафиолета. 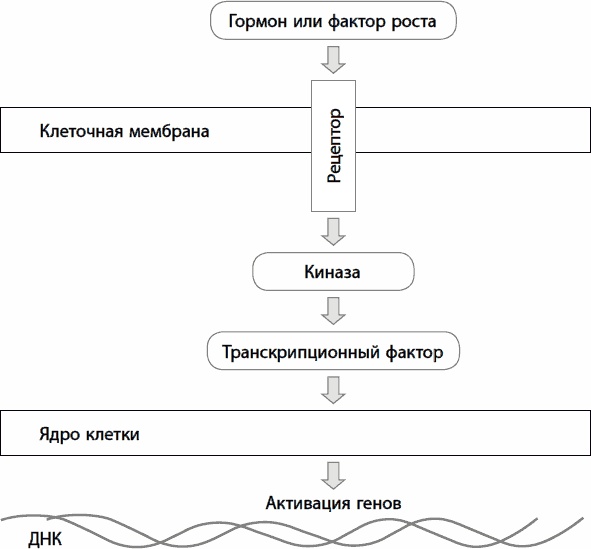
Рис. 4. Схема программирования активности генов клетки гормонами Белки животного происхождения, киназа mTOR и аутофагия
Проведенные на протяжении 32 лет наблюдения показали, что употребление животных белков увеличивает общую смертность, особенно это касается переработанного красного мяса и яиц. Красное мясо наиболее значимо увеличивало смертность людей от сердечно-сосудистых заболеваний. Растительный белок, наоборот, снижал смертность в среднем на 10 % на каждые 3 % повышения доли в рационе. Давно было известно, что ограничение до необходимого минимума употребления метионина – незаменимой аминокислоты, которой больше всего в продуктах животного происхождения, увеличивает максимальную продолжительность жизни экспериментальных мышей и крыс до 40 % и выше. Избыток метионина в нашем теле переходит в гомоцистеин, который увеличивает риск атеросклероза и сердечно-сосудистых заболеваний. Кроме того, метионин снижает уровни «гормонов долголетия» адипонектина, FGF21 и увеличивает «гормоны старения» лептина, IGF-1. Некоторые аминокислоты, которыми наиболее богаты животные пищевые белки (лейцин, аргинин, лизин), вызывают активацию киназы mTOR. Этот белок считается важнейшим переключателем клеточных программ. Когда пищи достаточно, mTOR активирует процессы биосинтеза нужных для роста клетки белков и создание новых «фабрик по сборке белков» – рибосом. Когда пищи очень много, вновь образуемых белков становится столько, что клетка не успевает их рассортировывать в особых «трубопроводах», которые называются эндоплазматической сетью. Некоторые вновь синтезированные белки не могут принять рабочую форму, сбиваются в агрегаты. Возникает стресс эндоплазматической сети, приводящий к старению или гибели клетки. С другой стороны, mTOR отключает за ненадобностью очень важный процесс, который называется аутофагией. В результате этого процесса клетка освобождается от скопившегося мусора – агрегатов белков, окисленных жиров, поврежденных структур, например отработавших свой век клеточных «электростанций» – митохондрий. Отключение аутофагии останавливает самоочищение клеток и регенерацию тканей. Например, установлено, что без активации аутофагии невозможно образование новых мышечных волокон. С одной стороны, стресс эндоплазматической сети, с другой – выключение аутофагии. Вот та плата, которую мы платим за переедание животных белков. А что будет, если приглушить активность киназы mTOR? Генетические исследования, проведенные на животных, показали, что это эффективный способ замедлить старение и продлить жизнь, но при этом страдает качество жизни, так как контролируемые mTOR процессы важны для клеток. Были найдены вещества-ингибиторы, подавляющие активность mTOR. Прием одного из таких препаратов в экспериментах на средневозрастных мышах позволил продлить жизнь на 20 %. Однако не обошлось без побочных эффектов, связанных с необходимостью некоторого уровня активности mTOR для клетки. В этих экспериментах использовались вещества, очень сильно подавляющие активность mTOR. Однако во многих продуктах питания есть менее селективные ингибиторы, с меньшей эффективностью подавляющие mTOR (табл. 22). И это залог меньших побочных эффектов для роста клеток и регенерации тканей.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно