
|
||
|
|
||
|
|
Онлайн книга - Наука воскрешения видов. Как клонировать мамонта | Автор книги - Бет Шапиро
Cтраница 33

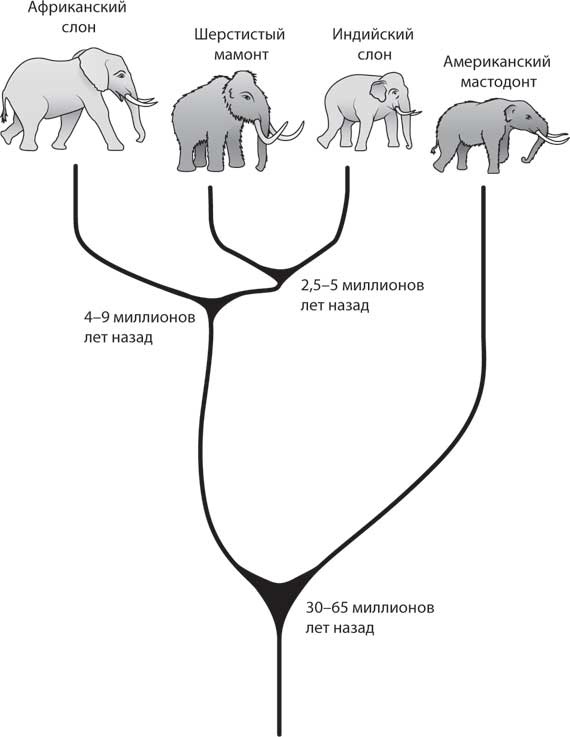
Рис. 9. Эволюционные связи между мамонтами, мастодонтами, а также индийскими и африканскими слонами, основанные на изучении ископаемых останков и последовательностей митохондриальной ДНК этих животных Проще всего будет соединить те кусочки пазла, которые относятся к наиболее сохранившимся участкам генома. Это части генома, общие или почти общие для мамонтов и современных слонов, да и всех видов млекопитающих. Мы наверняка справимся и с кусочками, относящимися к тем частям генома, в которых мамонты и африканские слоны похожи, хотя и не полностью идентичны. Сложнее всего будет собрать фрагменты, принадлежащие областям генома, в которых различия между мамонтами и африканскими слонами очень велики. Такие расхождения могут быть следствием перестановки или даже удвоения или исчезновения генов. В книге «Парк юрского периода» ученые заполнили пробелы в геноме динозавра – на месте фрагментов, которые они не смогли секвенировать, – с помощью ДНК лягушки. Точно так же мы можем решить эту проблему, просто заполнив недостающие участки при помощи ДНК слона. Но вряд ли это хорошая идея. Общий предок мамонтов, индийских слонов и африканских слонов жил на Земле около 4 миллионов лет назад. Это значит, что мамонта отделяет от индийского и африканского слонов более 8 миллионов лет эволюционных изменений – достаточно длинный промежуток, чтобы успели накопиться эволюционные различия. Одними из самых трудных в сборке будут те области генома мамонта, которые подверглись изменениям после точки расхождения мамонтов и других видов слонов. Вероятно, эти участки будут относиться к наиболее важным областям генома, которые потребуется изменить, чтобы получить слона, выглядящего и ведущего себя как мамонт, а не как слон. С точки зрения возрождения вымершего вида узнать правильную последовательность нуклеотидов в этих областях генома будет важнее всего. В случае геномов живых видов лучший способ собрать эти наиболее каверзные участки заключается в том, чтобы секвенировать очень длинные фрагменты ДНК. Под «длинными» я имею в виду участки длиной в тысячи и сотни тысяч спаренных оснований. Сделать это сложно, и на попытки каждый год уходят огромные деньги. К сожалению, длинные цепочки древней ДНК не сохраняются: большинство наших фрагментов содержат менее сотни спаренных оснований, а зачастую и намного меньше. Так что даже если в ближайшие несколько лет у нас произойдет технологический прорыв, позволяющий секвенировать очень длинные участки ДНК, это не принесет особой пользы для возрождения вымерших видов. Хорошая новость заключается в том, что стоимость секвенирования ДНК продолжает снижаться, а значит, мы можем создавать все больше и больше цепочек ДНК каждого нашего древнего образца, не разоряясь при этом до основания. Кроме того, мы совершенствуем способы выделения ДНК из окаменелостей. Несмотря на то что эти фрагменты будут короткими, их количество может увеличиться. Кроме того, если нам повезет, мы найдем древние образцы (к примеру, сохранившиеся в замерзшей арктической почве), содержащие много сотен спаренных оснований, – хотя крайне маловероятно, чтобы нам удалось обнаружить фрагменты длиной в тысячи или сотни тысяч спаренных оснований. Наконец, совершенствуются вычислительные методы, используемые для соединения фрагментов ДНК при отсутствии близкородственного шаблонного генома, что позволит нам получить более качественные сборки древних геномов все более разнообразных видов. Правда, однако, заключается в том, что ни один геном млекопитающего еще не был секвенирован полностью. Это касается и человеческого генома, хотя появившиеся более 10 лет назад восторженные заявления определенно указывают на обратное. Правда заключается в том, что отдельные участки человеческого генома до сих пор не были секвенированы, и их нельзя секвенировать ни одним из существующих способов. Геном состоит из двух компонентов: эухроматина – компонента, содержащего гены, и гетерохроматина – очень плотного компонента, состоящего из повторяющихся фрагментов. В эухроматической части человеческого генома все еще присутствует несколько очень маленьких несеквенированных промежутков, но на них приходится менее 1 % генома. Вторая, более крупная недостающая часть относится к гетерохроматическим участкам. Гетерохроматин составляет около 20 % человеческого генома, и поскольку он содержит множество повторяющихся фрагментов, это наиболее сложная для секвенирования часть человеческого (и вообще любого) генома. Гетерохроматин, вероятно, играет важную роль в регуляции экспрессии генов, направляя сегрегацию хромосом во время деления клетки и определяя, где разные хромосомы должны находиться в ядре. Но поскольку с помощью существующих технологий секвенировать его очень трудно, мы знаем о гетерохроматине намного меньше, чем о эухроматической части генома. Секвенировать гетерохроматин из древнего образца будет не легче, чем в случае живого человека. На самом деле секвенировать гетерохроматин из образца, находящегося в плохом состоянии, скорее всего, окажется намного сложнее, чем из образцов тканей живых организмов, вследствие фрагментации древней ДНК. Станет ли это серьезным препятствием на пути к возрождению вымерших видов, еще предстоит выяснить. Поскольку нам не удастся узнать полную геномную последовательность вымершего вида, синтезировать геном целиком с нуля при возрождении вымершего вида не получится, даже если у нас появится возможность воссоздать искусственную эукариотическую жизнь. Но я совершенно уверена, что синтетическая биология – это действительно способ возродить вымершие виды и исчезнувшие признаки. Пусть нам не удастся создать целый геном, но ведь мы можем синтезировать фрагменты ДНК. Что, если мы используем эти фрагменты, чтобы вернуть вымершие виды к жизни путем редактирования генома? Вырезать и вставить мамонта
Джордж Чёрч – преподаватель генетики в Гарвардской медицинской школе и ведущий участник еще одного проекта по возрождению мамонта. Этот проект заметно отличается от тех, организаторы которых рассчитывают обнаружить нетронутые клетки в вечной мерзлоте Сибири. Для воскрешения мамонта Джордж использует редактирование генома, которое, как я уже говорила, представляет собой один из двух доступных нам способов восстановления исчезнувших признаков. Я познакомилась с Джорджем в 2012 году в Институте Висса в Кембридже, штат Массачусетс. Он принимал у себя мини-конференцию, организованную Райаном Феланом и Стюартом Брандом из фонда Long Now в рамках их некоммерческой инициативы Revive & Restore. Формально конференция была посвящена проекту по возрождению странствующего голубя, и, как ученый, чья лаборатория исследования древней ДНК содержит наиболее обширную коллекцию останков странствующих голубей, я тоже получила приглашение. Кроме того, на конференции присутствовали специалисты в области природоохранной биологии, в том числе Ноэль Снайдер из Службы охраны рыбных ресурсов и диких животных США, который посвятил много лет проекту по охране калифорнийского кондора, а также ученые, работающие в сфере биоэтики, к примеру Хэнк Грили, преподаватель права в Стэнфордском университете, специализирующийся на социальных и этических последствиях применения биотехнологий. Обсуждение было напряженным и временами велось на повышенных тонах, но оно принесло огромную пользу: именно на этой мини-конференции я поняла, как именно должно свершиться восстановление вымерших видов.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно