
|
||
|
|
||
|
|
Онлайн книга - Лаборатория химических историй. От электрона до молекулярных машин | Автор книги - Михаил Левицкий
Cтраница 35

Упрощение бывает полезно
До сих пор мы обсуждали только атомы, а теперь перейдем к молекулам. Вернемся к молекуле метана CH4, изображенной на обложках учебников (рис. 4.3). У атома углерода на втором электронном уровне находятся четыре орбитали (одна s и три р). На них расположены четыре валентных электрона: два – на s-орбитали и еще по одному электрону – на двух р-орбиталях, третья р-орбиталь углерода не занята. В тот момент, когда атом углерода образует четыре химических связи с четырьмя атомами водорода, все четыре орбитали сливаются, образуя орбитали-гибриды (рис. 4.19, справа внизу), которые по форме напоминают несимметричные объемные восьмерки (крупная капля и маленький хвостик). Обычно их обозначают как sp3-гибридные орбитали, то есть полученные из одной s- и трех р-орбиталей (орбиталей-гибридов получится столько же, сколько орбиталей участвует в слиянии). Своими утолщенными частями гибридные орбитали направлены к вершинам мысленного тетраэдра (рис. 4.19, справа внизу). 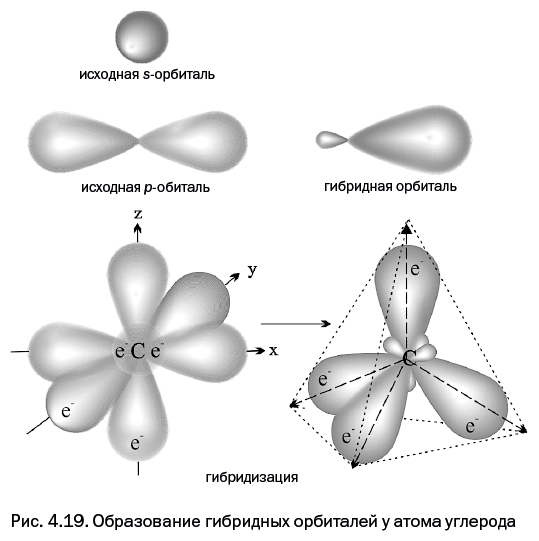
Такие картинки можно увидеть во всех учебниках органической химии, а истинный внешний вид гибридов показан на рис. 4.20. Для того чтобы нагляднее показать их форму, гибриды изобразили на некотором удалении друг от друга (рис. 4.20, слева), но чтобы увидеть всю картину в реальности, эти орбитали необходимо совместить в пространстве – при этом четыре белые точки должны совпасть (именно в этом месте находится ядро углерода). Результат показан на рис. 4.20, справа. 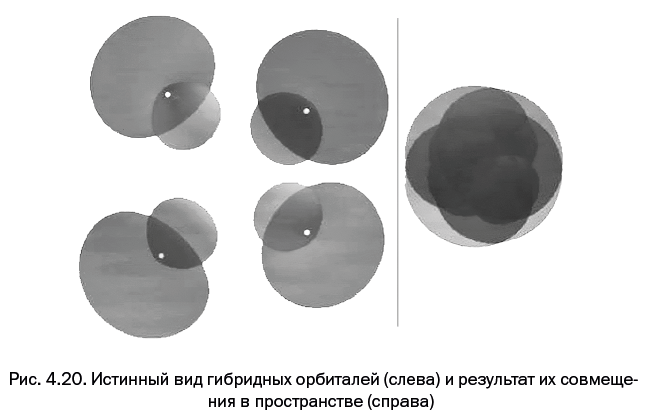
Далее эти четыре орбитали, направленные к вершинам мысленного тетраэдра, перекрываются со сферическими орбиталями четырех атомов водорода, что соответствует образованию четырех химических связей (как показано на обложках учебников). Именно здесь возникают сложности с графическим изображением: если к фигуре, состоящей из «слипшихся» шарообразных объемов (рис. 4.20, справа), вплотную приблизить четыре сферы, то разобрать на рисунке ничего не удастся. Все выглядит намного понятнее, если гибридные орбитали намеренно растянуты (рис. 4.19). Поэтому истинный вид орбиталей постоянно искажают в угоду наглядности, и на это трудно что-либо возразить. Впрочем, рис. 4.20 поможет любителям точности представить, как все выглядит на самом деле. Рисунки на обложках учебников изображают перекрывание орбиталей атомов углерода и водорода в молекуле метана, но это промежуточная стадия, наиболее часто изображаемая и обсуждаемая. Когда связи уже образовались, появляются молекулярные орбитали, очерчивающие области возможного перемещения электронов вокруг молекулы. Число молекулярных орбиталей равно сумме исходных атомных орбиталей. На рис. 4.21а показана одна из молекулярных орбиталей метана. 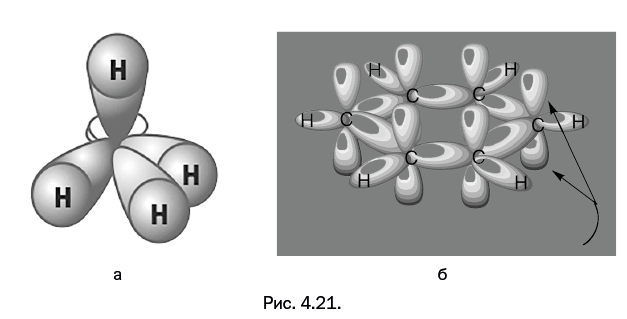
Во многих случаях химиков интересуют именно молекулярные орбитали, которые так же, как атомные орбитали, получают расчетом. На первый взгляд показанные объемные конструкции не имеют отношения к экспериментальной химии, однако это не так. Перекрывание атомных р-орбиталей в бензоле приводит к образованию единого кольцевого облака (рис. 4.21б – орбитали, охватывающие атомы водорода, не показаны). Это кольцевое облако и является основным признаком ароматических свойств. Кроме того, взаимоперекрывание орбиталей в пределах одной молекулы часто определяет электропроводящие или магнитные свойства вещества. Возможность протекания некоторых реакций определяется взаиморасположением молекулярных орбиталей в реагирующих молекулах – сформулированы соответствующие правила, и химики-синтетики их учитывают. И то, что все это хорошо согласуется, подтверждает близость результатов квантово-химических расчетов к реальности. Глава 5
От колбы к компьютеру Начало ХХ в. было отмечено большими успехами в физике – и прежде всего созданием квантовой механики. В 1900 г. появилась работа немецкого физика Макса Планка, лауреата Нобелевской премии 1918 г. по физике, в которой он утверждал, что у элементарных частиц любая энергия (в том числе и световая) поглощается или испускается только дискретными порциями – квантами (от лат. quantum – «порция»). Минимальное количество световой энергии – квант света – получило название "фотон". Интересно, что Планк считал свою теорию лишь математическим упражнением, лишенным какого-либо физического смысла, однако физики довольно быстро нашли ей применение. В 1913 г. датский физик Нильс Бор, будущий лауреат Нобелевской премии 1922 г. по физике, применил теорию квантов к объяснению строения атома, что привело к формированию нового раздела физической науки – квантовой механики. Естественно, такое событие не могло не затронуть химию, что вскоре и произошло. Еще одна химия
Постепенно химиков перестал удовлетворять обычный эксперимент, и возникла идея применить расчеты для определения структуры молекулы. Все чаще вставал вопрос о том, каковы будут свойства молекулы, которая пока не синтезирована, а только нарисована на бумаге. Ответы на эти вопросы сегодня может дать квантовая химия, о которой будет рассказано ниже. Квантовая химия родилась в недрах более общей науки – квантовой механики. Далеко не сразу эта новая наука получила широкое признание ученых, поскольку она противоречит житейскому здравому смыслу, который основан на нашем повседневном опыте взаимодействия с окружающими предметами. Обычно мы имеем дело с весьма крупными объектами, состоящими из многих миллиардов молекул, но у нас нет опыта, связанного с одиночными атомами и молекулами, и потому их поведение, описываемое квантовой механикой, кажется порой нелогичным. Например, электрон можно рассматривать и как частицу, и как волну, хотя в обычном мире это разные понятия. Пример частицы, несущей энергию, – это летящий камень, но волна в нашем понимании – нечто иное. Мы видим волны при колебании водной поверхности, распространение звука тоже волновой процесс. Именно такое необычное сочетание свойств стало причиной конфликта, в результате которого возникла отдельная ветвь химии – квантовая химия. В 1926 г. австрийский физик Эрвин Шрёдингер, будущий лауреат Нобелевской премии по физике 1933 г., выступал на научном семинаре в Цюрихском университете, где рассказывал о новых идеях, утверждая, что объекты микромира ведут себя и как волны, и как частицы. По легенде, распространенной среди физиков, в результате слова попросил пожилой преподаватель, который сказал: "Шрёдингер, вы что, не видите, что все это чушь? Или мы тут все не знаем, что волны – они на то и волны, чтобы описываться волновыми уравнениями?" [10]. Самолюбивый Шрёдингер воспринял замечание как личную обиду и решил разработать волновое уравнение, описывающее поведение частиц в рамках квантовой механики. Шрёдингер справился с задачей, и в результате появилось знаменитое волновое уравнение, которое позволяет описать область пространственного расположения электрона у атомного ядра – а точнее, вероятность нахождения частицы в заданной точке пространства. На этом Шрёдингер не остановился – он решил показать применимость своего уравнения и предложил двум немецким физикам Фрицу Лондону и Вальтеру Гайтлеру провести расчет молекулы водорода на основе волнового уравнения. Расчет показал, что при образовании из двух атомов молекулы водорода электрон, принадлежавший первоначально одному из атомов Н, будет также принадлежать и другому, то есть атомы обобществляют свои электроны, что лежит в основе понятия о ковалентной связи. Проведенный расчет имел огромное значение для дальнейшего развития химии: впервые удалось показать, что с помощью квантовой механики можно понять природу химической связи. 1927 год считают годом зарождения квантовой химии.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно