
|
||
|
|
||
|
|
Онлайн книга - Карнавал молекул | Автор книги - Михаил Левицкий
Cтраница 35

Подводя итоги, отметим, что использование металлоценовых и постметаллоценовых катализаторов позволяет синтезировать полимеры с широким диапазоном свойств, а также варьировать жесткость и эластичность материала. Можно предположить, что эти катализаторы, «дирижируя» расположением звеньев в полимерной цепи, позволят в будущем создавать целые «оркестры» новых, уникальных по свойствам материалов, которые сумеют занять лидирующее место в полимерной эстафете. 4
Корзина пестрых фактов Крохотный факт стоит целого сонма несбыточных грез. РАЛФ ЭМЕРСОН Химия безусловно истинная наука, в ней много накопленных результатов, законов и правил, но всегда есть место неожиданностям. Бывает, что сложившиеся представления прочно укореняются в сознании и необычный факт, который не согласуется с общепринятыми понятиями, воспринимается с недоверием или как чудо. Все же у химиков хватает терпения, чтобы во всем разобраться и поставить все на свои места. Рассмотрим, как то, что казалось невозможным, все же удалось осуществить. Исправим учебник химии
Только не обещайте исправить положение вещей, а то опять каких-то вещей не досчитаемся! МИХАИЛ МАМЧИЧ Сразу отметим, что этот случай – исключительно редкий. В учебниках содержатся знания, отшлифованные и проверенные десятилетиями, однако бывают сюрпризы. Например, известно, что угольная кислота Н2СО3 в свободном виде не существует, она быстро распадается с образованием CO2 и воды, что мы часто можем наблюдать, открывая газированные напитки. Вот цитата из учебника «Начала химии» (авторы Н.Е. Кузьменко, В.В. Еремин, В.А. Попков): «…свободная угольная кислота неизвестна, так как она неустойчива и легко разлагается…». Результат был проверен столь многократно, что не вызывал никаких сомнений, потому не будем никого укорять за ошибку, поскольку до определенного момента это считалось истиной. Современные исследования показали, что в это утверждение можно внести поправку. Угольную кислоту Н2СО3 как индивидуальное соединение удалось получить при нагревании в высоком вакууме бикарбоната аммония (рис. 4.1). 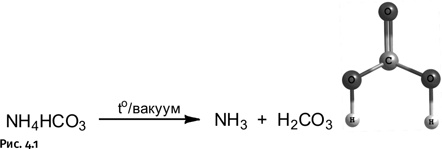
Стабильность чистой H2CO3 достаточно высока, она может возгоняться в вакууме, но ее разложение при нагревании все же возможно. При любом превращении реагирующие молекулы вначале образуют некое промежуточное соединение (так называемый переходный комплекс), которое затем распадается, образуя продукты реакции. Образование комплекса требует затрат энергии. Чем меньше эта энергия, тем легче проходит реакция. Разложение угольной кислоты при нагревании проходит через циклический переходный комплекс, образуемый четырьмя атомами О-С-О-Н. Цикл возникает благодаря так называемой водородной связи между атомами О и Н (на рис. 4.2 показана пунктиром): Энергия образования такого комплекса 184 кДж/моль. 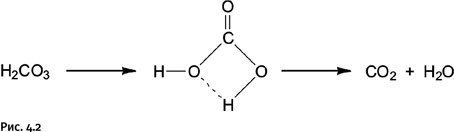
В присутствии воды, т. е. при обычном способе получения угольной кислоты, легко образуется восьмичленный переходный комплекс с помощью тех же водородных связей при участии одной молекулы угольной кислоты и двух молекул Н2О. Энергия образования такого комплекса почти вдвое меньше, 100 кДж/моль, и разложение проходит очень быстро (рис. 4.3). 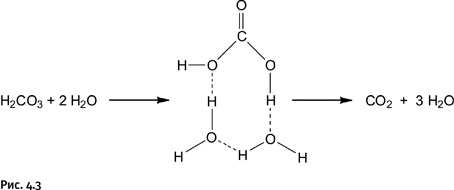
Возможность существования угольной кислоты в свободном виде не только интересна, но и важна, это открытие позволило по-новому взглянуть на процесс дыхания. Полагают, что в живом организме угольная кислота, «оберегаемая» от разложения специальным ферментом, позволяет осуществлять быстрый перенос углекислого газа из клеток в кровь, а затем мы его выдыхаем через легкие. Поскольку свободная угольная кислота получена и, естественно, изучен ее спектр, астрономы полагают, что теперь она может быть спектрально обнаружена в атмосфере планет Солнечной системы. Полувековая иллюзия
Все иллюзия. Конечно, и предыдущая фраза. СТАНИСЛАВ ЕЖИ ЛЕЦ С момента открытия в конце XIX в. благородных газов (He, Ne, Ar, Kr, Xe) они считались химически абсолютно пассивными и не способными вступать в какие-либо реакции, поэтому их назвали инертными. Такая точка зрения продержалась вплоть до 1962 г., однако в результате работ канадского ученого Нила Бартлетта (рис. 4.4) эти представления пришлось пересматривать. 
Изучая соединение платины с фтором PtF6, Бартлетт обратил внимание на сильнейшие окислительные способности этого соединения, оно способно окислять даже молекулярный кислород, который сам хороший окислитель. В результате получается соединение, в котором у кислорода изъят один электрон и он получает положительный заряд O2+[PtF6]–. Бартлетту пришла в голову интересная мысль: если гексафторид платины может оторвать электрон от кислорода, то он может проделать то же самое с ксеноном, поскольку, как уже было известно, для этого требуется несколько меньшая энергия, чем в случае кислорода. В результате опыта он получил сразу несколько химических соединений переменного состава, содержащих ксенон (рис. 4.5 и 4.6). 
Это сообщение сразу привлекло внимание химиков. Оказалось, что фторировать ксенон можно и без участия платины действием элементарного фтора. Так были получены XeF4 и XeF6. Фтор настолько сильный окислитель, что способен отрывать электроны даже от устойчивой восьмиэлектронной оболочки инертного газа. На этом исследователи не остановились, удалось даже получить кислородные соединения ксенона, например XeO3. Таким образом миф, утверждавший абсолютную инертность благородных газов, удалось разрушить. Возникло не только новое направление в химии, это открытие привело к пересмотру некоторых фундаментальных представлений. Нулевую группу в периодической системе упразднили, а благородные газы поместили в VIII группу, т. е. туда, где находятся малоактивные благородные металлы палладиевой и платиновой групп. 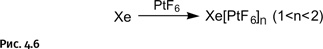
Прокатиться на реакции
Хорошо кататься по российским просторам
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно