
|
||
|
|
||
|
|
Онлайн книга - На грани возможного. Наука выживания | Автор книги - Фрэнсис Эшкрофт
Cтраница 79

Вторая трудность, которую приходится преодолевать животным, промерзающим целиком, – это обезвоживание и съеживание клеток при замерзании межклеточной жидкости. Оно чревато денатурацией клеточной мембраны и повреждением клеточного белка, а замерзание более 65 % жидкости организма ведет к летальному исходу. Изменений в клеточном объеме морозостойкие животные избегают, повышая уровень сахара или аминокислот в клетках. Эти криопротекторы снижают образование льда и потерю клеточной жидкости, а также стабилизируют мембрану, позволяя ей выдерживать большую степень съеживания без повреждений. В число криопротекторов входит и глицерин, и сахар – например, трегалоза (у насекомых) или глюкоза (у лягушек). Размораживание, как и заморозка, тоже не пускается на самотек. Например, когда оттаивают перезимовавшие во льду лягушки, сперва размораживается сердце, что обеспечивает восстановление самых необходимых жизненных функций и ускоряет процесс размораживания, разгоняя теплую кровь по телу. Анабиоз
Новейшие технологии позволяют сравнительно легко охлаждать клетки и ткани млекопитающих до весьма низких температур. Термин «криоконсервация» происходит от греческого kryos – ледяной холод. При низкой температуре метаболические процессы в клетках настолько замедляются, что организм впадает в состояние анабиоза, и клетки сохраняются гораздо дольше, чем позволяет их естественная продолжительность жизни. Чем ниже температура, тем медленнее метаболизм, а значит, дольше можно сохранить клетки. Для того чтобы не допустить обезвоживания или формирования кристаллов льда, скорость замерзания и размораживания должна строго контролироваться, и в раствор, в котором хранятся клетки, необходимо добавлять криопротекторы. Обычно используется глицерин, поскольку он препятствует превращению воды в лед даже при температуре жидкого азота. В жидком азоте при температуре менее –196° С замораживают сперму для искусственного оплодотворения. Изначально технология разрабатывалась для крупного рогатого скота, однако уже в 1953 г. ее успешно применили для замораживания спермы человека. Замороженные образцы спермы сохраняют свои свойства десятилетиями, и человеческая сперма, пролежавшая в заморозке 15 лет, успешно послужила для зачатия. Многие мужчины стараются сохранить свою сперму перед вазэктомией, а также химиотерапией или лучевой терапией, которые убивают сперматозоиды. Другие сдают сперму для бесплодных пар. От прошедших заморозку образцов спермы ежегодно рождаются тысячи младенцев, и оплодотворение такой спермой, по имеющимся данным, чаще приводит к зачатию, чем оплодотворение свежей спермой. 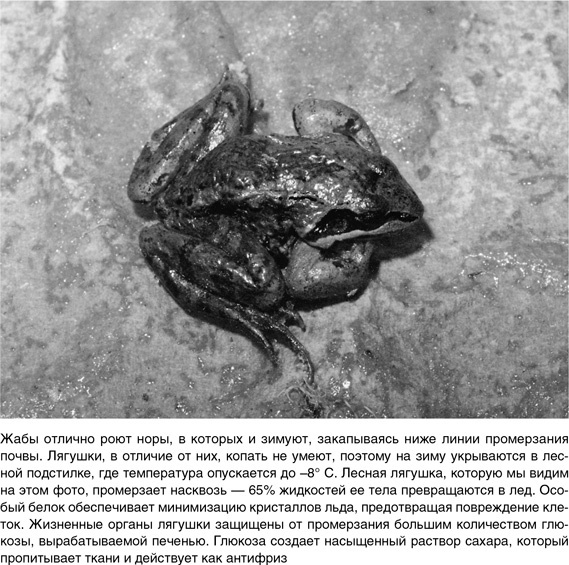
Замораживанием при низкой температуре можно сохранять и эмбрионы. Отработанная сперва на домашних животных, сегодня эта технология входит на обычной основе в процедуру ЭКО (экстракорпорального оплодотворения) у людей. Обычно в процессе операции у женщины забирается несколько яйцеклеток, оплодотворяется in vitro, а затем два или три эмбриона подсаживаются в матку. Неиспользованные эмбрионы замораживаются, на случай если первые не приживутся. Таким образом, женщине не приходится повторно проходить процедуру взятия яйцеклеток, а кроме того (поскольку эта процедура – самая дорогостоящая часть операции), снижается стоимость последующих попыток ЭКО. «Запасные» эмбрионы могут храниться в течение нескольких лет, позволяя паре через какое-то время завести при желании и второго ребенка. Они также могут понадобиться, если женщине придется проходить медицинские процедуры, способные снизить ее фертильность, или даже для других женщин, у которых не вырабатываются собственные яйцеклетки. Первым ребенком, родившимся из замороженного эмбриона, стала Зоуи Лейленд – она появилась на свет 28 марта 1984 г. в австралийском Мельбурне. На сегодняшний день отмечено не одно успешное развитие беременности с эмбрионами, пролежавшими замороженными пять лет. 
Поддаются замораживанию и другие клетки человеческого тела. Самые знаменитые – это, конечно, клетки HeLa, выделенные из раковой опухоли пациентки по имени Henrietta Lacks (отсюда и название) и немедленно замороженные в жидком азоте. Сегодня, спустя много лет после смерти пациентки, потомков изначальных клеток можно обнаружить в исследовательских лабораториях по всему миру, где они используются в качестве ценного научного материала. Если отдельные клетки млекопитающих можно замораживать и размораживать практически без последствий, это не значит, что подобную процедуру выдержит организм целиком. В США уже сейчас существует несколько фирм, занимающихся криоконсервацией. Они замораживают тела (или головы) недавно усопших, в надежде, что когда-нибудь в будущем технологии позволят их правильно разморозить, вылечить, заменить «изношенные» части тела и их жизнь продолжится с чистого листа. Большинство таких компаний располагается в Калифорнии, где законы, касающиеся криоконсервации, наименее жесткие. К сожалению, мечты клиентов пока далеки от осуществления, поскольку ткани человеческого тела после смерти быстро повреждаются, лишившись притока крови. Однако в каком-то смысле сохранить человека с помощью замораживания все же можно. Сохраняется его уникальный геном, совокупность генов организма. Для этого необходимо всего несколько клеток, которые можно взять, например, из пробы крови (эритроциты принадлежат к безъядерным клеткам, поэтому не содержат ДНК, все же в крови найдется достаточно лейкоцитов, чтобы обеспечить необходимую генетическую информацию). Возможно, когда-нибудь мы научимся восстанавливать человека из единственного лейкоцита – с помощью тех же технологий, благодаря которым удалось клонировать знаменитую Долли. Насколько это будет этически оправдано – другой вопрос. Однако не стоит забывать, что даже при удачном развитии событий клон, полученный из этой единственной клетки, будет вашей копией не больше, чем однояйцевый близнец. Ведь индивидуальность – это не просто набор генов. Миллионное состояние на микробах
Экстремофилы превращаются в прибыльный бизнес. Основу развития этого рынка составляют ферменты, выделенные из организмов, способных переносить экстремальный холод, жару, соленость, кислотность, давление, тяжелые металлы и многие другие крайности. Представители фирм, занимающихся исследованиями в области биотехнологий, отправляются на край света в поисках новых экстремофилов, которые могут содержать неизвестные доселе гены, а затем мчатся со всех ног патентовать свои открытия. Потенциальная прибыль огромна, поэтому конкуренция в этой области жесткая. Тысячи молекулярных биологов ежедневно пользуются в своих исследованиях способностями гипертермофилов. Жаростойкие ферменты применяются для того, чтобы в процессе под названием ПЦР (полимеразная цепная реакция) размножить выбранный фрагмент ДНК. Как нетрудно догадаться, этот процесс подразумевает повторяющиеся один за другим реакционные циклы. Сперва ДНК требуется нагреть, чтобы разделить на две составляющие цепочки. Затем ее охлаждают и каждую цепочку реплицируют с помощью фермента. Эти два шага многократно повторяют, обеспечивая рост числа молекул ДНК в геометрической прогрессии. В основе метода ПЦР лежит использование фермента ДНК-полимеразы, который не распадается при высоких температурах (95° С), необходимых для разделения двух цепочек ДНК. К счастью, именно такими свойствами обладают гипертермофильные ферменты, в том числе и Taq-полимераза, применяющаяся в ПЦР. Метод ПЦР имеет и прикладное значение, он широко используется в медицине – например, для определения бактериальных штаммов или генетических обследований. Кроме того, он совершил настоящий переворот в криминалистике: для производства миллиона копий ДНК по технологии ПЦР достаточно всего нескольких молекул, поэтому теперь преступника можно установить по одной-единственной клетке, оставленной на месте преступления.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно