
|
||
|
|
||
|
|
Онлайн книга - 120 лет жизни – только начало. Как победить старение? | Автор книги - Алексей Москалев
Cтраница 40

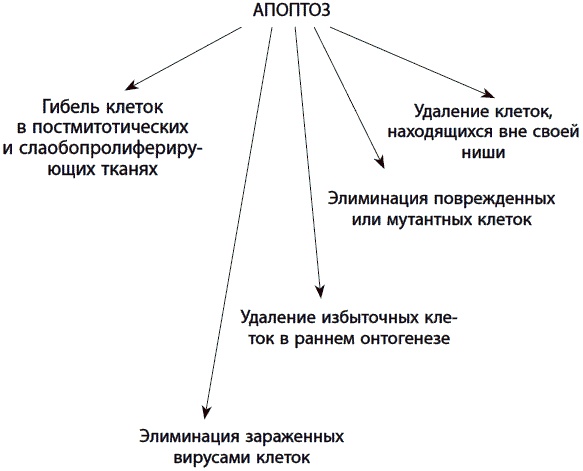
Рис. 25. Функции апоптоза в индивидуальном развитии и старении Возможны несколько способов участия апоптоза в процессе старения. Во-первых, позитивный, через устранение опухолевых и поврежденных стареющих клеток (например, фибробластов и клеток печени), которые затем могут быть заменены путем деления; таким образом, сохраняется тканевый гомеостаз. Во-вторых, утрата постмитотических клеток (например, нервных клеток или клеток сердечной мышцы), которые не могут быть заменены, что ведет к патологии. В третьих, при старении отдельные типы клеток теряют способность подвергаться апоптозу, что может служить причиной избыточного накопления нефункциональных стареющих клеток, аутоиммунных заболеваний (таких, как ревматоидный артрит) или опухолевого процесса. Таким образом, частью феномена старения может являться как увеличение чувствительности клеток к апоптозу, так и снижение, то есть тканеспецифическая разрегулировка апоптоза. Истощение количества стволовых клеток Развитие каждого индивида начинается с эмбриональных стволовых клеток. Даже самые примитивные многоклеточные организмы обладают стволовыми клетками. На ранних стадиях развития эмбриона из имеющихся клеток могут сформироваться любые клетки и ткани организма (несколько сотен типов). После первых нескольких делений зародыша стволовые клетки могут давать начало только некоторым, но не всем, клеточным линиям, а еще позже они могут становиться родоначальниками всего лишь нескольких определенных клеточных типов. Последняя группа стволовых клеток присуща, в небольшом количестве, и взрослому организму. Они обычно пребывают в состоянии покоя либо делятся симметрично (самовоспроизводятся), но при необходимости могут приступить к асимметричному делению, образуя клетки, из которых далее развиваются зрелые клетки, необходимые для функционирования той или иной ткани. Замена поврежденной клетки на новую в результате асимметричного деления стволовой клетки может обеспечить неограниченную устойчивость к дегенеративным изменениям любой ткани организма человека при условии, что сами стволовые клетки бессмертны. Однако этого не происходит. Почему стволовые клетки с возрастом реже самообновляются или неправильно созревают, а в других случаях, наоборот, начинают делиться бесконтрольно, превращаясь в раковые? На этот вопрос специалисты до сих пор не нашли однозначного ответа. Действительно, с возрастом способность стволовых клеток делиться и восстанавливать ткани снижается. Например, поседение вызывается уменьшением в волосяных мешочках количества стволовых клеток, вырабатывающих пигмент. Получены свидетельства постепенного спада репликативной способности кроветворных, кишечных и мышечных стволовых клеток. Таким образом, изменение функциональных возможностей стволовых клеток при старении — установленный факт. Снижение активности стволовых клеток способствует прогрессивному ухудшению регенерации тканей. Почему это происходит? Одни авторы считают, что стволовые клетки стареют «изнутри». Чем больше стволовые клетки взрослого организма делятся в течение жизни, тем больше они накапливают повреждений ДНК, в результате укорочения их теломер, стресса от «запутывания» при удвоении нитей ДНК, постепенного отказа систем починки ДНК, чрезмерного метилирования важных генов и активации «прыгающих» генов. Иногда при делении стволовой клетки даже теряются целые хромосомы. Другие авторы, напротив, полагают, что стволовые клетки потенциально бессмертны. Например, когда стволовые клетки половой системы, из которых возникают новые сперматозоиды, от старых самцов мышей последовательно пересаживали молодым особям в течение трех лет, заметного снижения их функции не наблюдалось, что косвенно свидетельствует о незначительном вкладе внутренних причин в старение данного типа стволовых клеток. Кроме того, сателлитные стволовые клетки мышц стареющих мышей продолжают выполнять свою функцию без изменений при условии, если присутствуют определенные системные факторы, получаемые при переливании крови от молодой мыши. Одной из причин повышенной жизнеспособности стволовых клеток по сравнению с другими типами клеток является активность особых транспортных белков, выбрасывающих из клеток поступающие в них токсины и избыточные гормоны. Кроме того, свойство бессмертия обеспечивается особой способностью перераспределять возникающие повреждения при асимметричном делении, когда одна дочерняя клетка остается стволовой, а вторая созревает в специализированную клетку данной ткани. Как было показано в специальных экспериментах, «клеточный мусор» — агрегаты окисленных и структурно неполноценных белков (агресомы), скапливающиеся в клетке, связаны только с одним из двух центров деления, вследствие чего при клеточном делении агресомы отходят лишь к одной из дочерних клеток. Как нетрудно догадаться, «клеточный мусор» достается созревающей клетке, а незрелая стволовая клетка за счет этого процесса очищается. По-видимому, при митозе стволовой клетки неслучайным образом распределяются не только поврежденные белки, но и родительская ДНК-матрица. Одним из следствий этого процесса может быть наблюдаемое снижение спонтанной частоты мутаций в стволовых клетках по сравнению с дифференцирующимися соматическими клетками, а также более медленное укорочение длины теломер. Теломеры могут укорачиваться и под действием окислительного стресса, поэтому некоторые стволовые клетки имеют активную теломеразу, при необходимости достраивающую концы хромосом. Правда, уровень активности теломеразы с возрастом падает даже в стволовых клетках, что, по мнению нобелевского лауреата Э. Блекберн, может служить маркером скорости старения у каждого конкретного человека. Таким образом, стволовая клетка «очищается» от внутриклеточного «мусора» и приобретенных в процессе репликации ДНК повреждений за счет образующейся созревающей клетки, что является менее энергозатратным и более надежным механизмом устранения повреждений, чем починка поломок, но обеспечивает более быстрое старение зрелых клеток. Возникло и другое предположение, согласно которому старение стволовых клеток, утрата способности к делениям запускается извне — в результате изменения гормонального фона и локального микроокружения стволовой клетки. Предположение о том, что стволовые клетки контролируются микроокружением, стимулирующим их самообновление и защищающим их от воздействий, вызывающих созревание, впервые было высказано в 1978 году и касалось кроветворных стволовых клеток. Экспериментально это предположение подтвердили значительно позже, когда было показано, что клетки костной ткани влияют на развитие кроветворных стволовых клеток, предоставляя им «инструкции» в виде сигнальных белков — факторов роста и цитокинов. Микроокружение стволовой клетки, необходимое для ее функционирования, получило название стволовой ниши. Помимо выполнения функции питания, стволовая ниша служит для стволовой клетки защитной и информационной средой. Она играет важную роль в обеспечении состояния покоя стволовой клетки и регулирует ее предрасположенность к вступлению на путь созревания в специализированную клетку. Структурно стволовая ниша представляет собой совокупность всех факторов, которые обеспечивают жизнеспособность и самовоспроизведение незрелых стволовых клеток, а также созревание дочерних специализированных клеток. К таким факторам относятся базальная мембрана, молекулы внеклеточного вещества, прочно закрепляющие стволовую клетку в нише, и определенные типы соседних клеток, продуцирующих факторы роста и различные регуляторные молекулы. В отличие от стволовых клеток, образующие стволовую нишу соседние клетки стареют с обычной скоростью. В свою очередь, клеточное старение, которому подвергаются клетки — соседи стволовой клетки, вызывает изменение спектра секретируемых ростовых факторов, провоцирует выделение цитокинов воспаления, мешающих состоянию покоя или самообновлению стволовых клеток, а также секрецию металлопротеиназ — ферментов, разрушающих внеклеточный матрикс.
|
 Вернуться к просмотру книги
Вернуться к просмотру книги
 Перейти к Оглавлению
Перейти к Оглавлению
 Перейти к Примечанию
Перейти к Примечанию
 © 2020 LoveRead.ec - электронная библиотека в которой можно
© 2020 LoveRead.ec - электронная библиотека в которой можно